Stanovenie hlavných ustanovení molekulárno-kinetickej teórie. Hlavné ustanovenia IKT. Vysvetlené Brownovi
Budeme mať dobrý pocit z rôznych vecí. Dokážeme to, ale je to ťažké, jazda alebo plyn. Vinikak lakomé jedlo o všetkom, čo nás opustí. Vidpovidi na bagato jedlo áno molekulárnej kinetickej teórie.
Molekulárno-kinetická teória je množstvo pohľadov na opis dôrazových schopností reči na základe vytvárania síl atómov a molekúl danej reči, interakcie módy.
Základné princípy teórie molekulovej kinetiky
Úsilie je uložené v časticiach – atómoch, molekulách, iónoch.
Používajú malé časti odchádzajú z neprerušovaného chaotického tepla Rus.
Medzi malými časticami, či už je to otázka sily, alebo v spojení s módou, je ťažké a vidshtovhuvannya.
V takom rangu, v molekulárnej kinetická teória o poslednom є systém, ktorý môže byť uložený z veľkého počtu častíc - makrosystém... Aby sme objasnili správanie takéhoto systému, zákony mechaniky neustrnú. K tomu je hlavným spôsobom komunikácie є štatistická metóda vivchennya orgány prejavu.
Pre objasnenie je pre šľachtu dôležité prenesenie výzorov základné charakteristiky molekúl:
- Rozmarín

Odhad veľkosti molekuly možno rozdeliť na veľkosť kocky a v ktorej je jedna molekula, kvôli sile pevných alebo hrubých slov a hmotnosti jednej molekuly:

- Molekuly Maca
Vidnoshennya masi prejav m na molekuly N od Daniy Rechovina:
- Typická molekulová hmotnosť
Hmotnosť molekuly (alebo atómu) danej reči je až 1/12 hmotnosti atómu v uhlíku:
- Počet prejavov
Počet prejavov a počet kusov N v til (atómy - v atómovej reči, molekuly - v molekule) na molekuly v jednom mole reči NA:

- Postiyna Avogadro
Počet molekúl, ktoré možno nájsť v 1 mole reči.
- Molárna masa
Molárna hmotnosť reči sa nazýva hmotnosť reči získaná z čísla 1 mol.
V medzinárodnom systéme rotuje jedna molárna hmotnosť reči kg / mol.
- Vzaєmodiya (iba na základe predpovedí)
Pre interakciu molekúl je charakteristická jedna hodina a ťažký čas a výstup: na stenách r
Molekulárno-kinetická teória dáva možnosť inteligencie, ktorá sa dá využiť v plynovom, hrubom a pevnom mlyne. Z pohľadu MKT má zabrať agregátová stanica Stredná hodnota priemerného počtu molekúl a povahy molekúl je jedna a tá istá.
Hlavné ustanovenia molekulárno-kinetickej teórie boli opakovane potvrdené fyzikálnymi experimentmi. Napríklad predtým:
A) Difúzia
B) Brownov ruch
Krátke tašky
Molekulárno-kinetická teória vysvetlí Budov a silu tilu na základe interakcie atómov, molekúl a iónov. Základ MKT spočíva tri polohy experimentálne aj teoreticky:
1) bolo potrebné skladovať v časticiach - molekulách, atómoch, iónoch;
2) časti rieky perebuyut pri neprerušovanom chaotickom horúčave rus;
3) medzi malými časticami je veľa sily alebo interakcie a je to ťažké a rýchle.
Molekulárni rečníci sú podporovaní bezprecedentnou priľnavosťou k molekulám v elektrónových mikroskopoch, ako aj odhodlaním pevnej reči na okrajoch, tvrdohlavou a prenikavou rečou. Thermal rox - hnedastý rox a difúzny. Prítomnosť intermolekulárneho vzájomného vzťahu medzi pružnosťou a pružnosťou pevných telies, povrchovým napätím ridinu.
Základné poznámky pred lekciou:

Jedlo na sebakontrolu podľa bloku „Základné princípy molekulárno-kinetickej teórie a їх donedávna“
- Formulujte hlavné tézy molekulárnej kinetickej teórie.
- Ako to, že opatrnosť a experimentovanie potvrdzujú základné princípy molekulárno-kinetickej teórie?
- Je to teda molekula? atóm?
- Čo sa nazýva prípustná molekulová hmotnosť? Aký je ohybový vzorec rozumu?
- Aký je názov čísla reči? Aký je ohybový vzorec rozumu? Yaka je jedno z mála slov?
- Ako nazývate Avogadro trvalým?
- Aká je molárna hmotnosť reči? Yakov vzorec ohýba zlé chápanie? Yaka je jedným z molárnej hmotnosti?
- Aká je povaha medzimolekulových síl?
- Aké silné sú molekulárne interakcie?
- Ako by sa mohli medzi nimi hromadiť?
- Opíšte povahu kolapsu molekúl v plynoch, líniách a pevných telesách.
- Aký je charakter balenia častíc v plynoch, pevných časticiach?
- Aký je priemer molekúl v plynoch, ridine a pevných časticiach?
- Zmeniť hlavný výkon plynov, ridin, pevných til.
- Čo sa nazýva Brownova veža?
- O tom, ako opraviť brownie ruch?
- Aký je názov difúzie? Na vedenie difúzie v plynoch, hrebeňoch a pevných telesách.
- 18. Ako položiť tekutosť difúzie od teploty do?
Molekulárno-kinetická teória je reťazec fyziky, ktorý je zodpovedný za silu starých rečových stavov a ako vysvetliť javy o objavovaní molekúl a atómov ako nájdených častí reči. IKT sú založené na troch základných ustanoveniach:
1. Usi reči sú uložené z nájdených častíc: molekúl, atómov a iónov.
2. Drobn castice prehlusuj nepreruen chaotick rus, ktorho rchlos je teplota prejavu.
3. Medzi malými časticami dochádza k ťažkému a ťažkému účinku, ktorého povaha leží v ich strede.
Hlavné ustanovenia IKT potvrdzujú ďalšie skutočnosti. Molekuly, atómy a ióny boli vychované experimentálne, molekuly boli odoberané a fotografované pomocou elektronických mikroskopov. Stav plynu nie je prepojený, aby expandoval a zaberal celú zásobu a dá sa vysvetliť neprerušovaným chaotickým kolapsom molekúl. Pružnosť plynov, pevných a tvrdých častíc, sila slabosti pevnej látky, procesy farmárčenia, lepenia, konzervovania tvorby pevných povrchov a o sile ťažkých molekúl a energie sa dá veľa hovoriť. Fenomén difúzie – schopnosť molekúl tej istej reči prenikať na rozhraní s inými molekulami – podporuje aj hlavné tézy MCT. Prejav difúzie vysvetľuje napríklad rozširovanie pachov, zmenu vývoja rôznych typov, proces rozhodovania pevných častíc na okrajoch, proces prerážania kovu spôsobom tavenia, alebo úchopom. . Na podporu neprerušovaného chaotického kolapsu molekúl є ako aj hnedastého rúna - neprerušovaného chaotického kolapsu mikroskopických častíc, nestráviteľných pri ridin.
Rukh hnedastých častíc sa vysvetľuje chaotickým drobením ridinových častíc, ktoré sa vkrádajú do mikroskopických častíc a nasmerujú ich na ruh. Mimochodom, bulo bolo informované, že frekvencia hnedastých častíc zostane pri teplote ridini. A. Einstein prelomil teóriu Brownovej rue. Vykonajte ruck častíc štatistického, imovirnіsnyho charakteru. Existuje len jeden spôsob, ako znížiť intenzitu hnedastého zákalu - zmeniť teplotu. Vzhľad hnedastého kormidla sa posúva na koniec molekúl.
Či už je reč zložená z častíc, počet reči sa berie úmerne k pomernému počtu častíc, tobto. konštrukčné prvky, scho sa pomstiť v tili.
Jeden počet slov je є krtek. Mole je celé číslo reči, teda pomstiť sa na štýle a štruktúrnych prvkoch či už ide o reč, alebo sa odohrávať v 12 g atómov v uhlíku C12. Pomer počtu molekúl reči k počtu molekúl reči sa nazýva Avogadrova postprodukcia:
Potom, čo Avogadro ukazuje, koľko atómov a molekúl možno nájsť v jednom mole reči. Molová hmotnosť je hmotnosť jedného mólu reči, čo je veľmi drahé pre množstvo reči k počtu reči:
Molárna hmotnosť sa uvádza v kg / mol. Keď poznáte molárnu hmotnosť, môžete vypočítať hmotnosť jednej molekuly:
Molárna hmotnosť je viazaná na prípustnú molekulovú hmotnosť Mg. Typická molekulová hmotnosť je hodnota, ktorá je vysoko relevantná pre hmotnosť molekuly danej reči až do 1/12 hmotnosti atómu v uhlíku C12. Yaksho vіdoma chemický vzorec reči, potom sa za doplnkovou mendelovskou tabuľkou dá priradiť k jednému z najbežnejších slov, jak, otočený v kilogramoch, ukáže veľkosť molárnej hmotnosti reči.
Obchodná hodnota 1
Molekulárna kinetická teória- cena rozpočtu a sila reči, založená na prejave atómov a molekúl, ako najpoužívanejšie častice chemických slov.
Hlavné ustanovenia molekulárnej kinetickej teórie molekuly:
- Všetky prejavy nájdete v hrubom, pevnom a plynovom mlyne. Zápach je vyrobený z častíc, ktoré sú uložené z atómov. Elementárne molekuly sa dajú zložiť, takže matky majú v sklade malý počet atómov. Molekuly a atómy sú elektricky neutrálne častice, pretože v spievajúcich mysliach nafúknu ďalší elektrický náboj a prenesú sa na pozitívne a negatívne.
- Atómy, ktoré sa molekuly zrútia bez prerušenia.
- Častice s elektrickou povahou sa spojili jedna po druhej.
Hlavné ustanovenia IKT a pažba nábojov sú znovu zakryté. Mіzh častice є maliy gravitatsіyny nalievanie.
Malunok 3. 1. 1. Traktorіya Brounіvskoy časť.
Obchodná hodnota 2
Brownov mol molekúl a atómov bol potvrdený. Dánsko tepelný rozpad častíc vykonávajú molekuly, ktoré sú dôležité v malých plynoch.
Predtým základné princípy molekulárnej kinetickej teórie
V roku 1827 sa rotsi R. Browna zmenili na plačúcu ploticu, ako búšenie bludov neopatrných úderov a premiestňovania molekúl. Oskіlki proces prichádza chaoticky, potom údery bohužiaľ nezmenia jeden. Vyzerá ako obrázok, ale jas časti koláčika nemôže byť trvalý, neustále sa mení, ale zobrazuje sa priamo v cikcakovom prehliadači, ktorý je zobrazený na malej 3. 1. 1.
O Brownovom ruhu hovoril v roku 1905 A. Einstein. Jógovú teóriu dokázali rozprávky J. Perrina z rokov 1908 - 1911.
Obchodná hodnota 3
Stopy Einsteinovej teórie: zmena štvorca< r 2 >hnedé časti klasu, spriemerované cez hnedé časti, úmerné hodine opatrnosti t.
Viraz< r 2 >= Dt Vysvetlím zákon difúzie. Pre teóriu maєmo, D monotónne rastie z vyšších teplôt. Za prejavmi difúzie je vidieť pustý ruch.
Obchodná hodnota 4
Difúzia- celá vec je prienik dvoch alebo niekoľkých rovnakých slov jedno v jednom.
Celý proces je rýchlo viditeľný v heterogénnom plyne. Difúzne pažby na zadok s malými gustinami môžu byť vyrobené ako jednoradové súčet. Ak viete v tej istej nádobe O 2 vodu a H 2 vodu s prepážkou, potom keď sú viditeľné plyny, opravia neporiadok, nie som v bezpečí. Proces je na hodinu náladový na presun do hôr a pod ním je kyslý.
Procesy vzájomného prenikania sa vyskytujú aj na cestách a stále viac. Akonáhle je razchiniti tvrdá, tsukor je blízko vody, potom sa rozpozná jednostranný razchin, ktorý є s primárnym zadkom difúznych procesov na ridins. o skutočné mysle Zmena hĺbok a plynov je maskovaná rýchlymi miešacími procesmi, napríklad v prípade konvekčného prúdenia.
Difúzia pevných telies naberá na svojej dôveryhodnej rýchlosti. Ak vyčistíte povrch kovu, môžete ho vyčistiť tak, že za hodinu je na koži atóm kovu.
Obchodná hodnota 5
Rozšírenie tejto hnedastej plotice je napadnuté spórovitými škodcami.
So vzájomne sa prenikajúcimi časticami koncov nie je mach sladký, takže je pravdepodobnejšie, že dôjde k chaotickému prenosu tepla molekúl.
Sily, ako výsledok dvoch molekúl, ležia zo všetkých ich strán. Molekuly majú vo svojom sklade kladné a záporné náboje. Vo veľkých časoch sú sily medzimolekulárnej záťaže premožené;
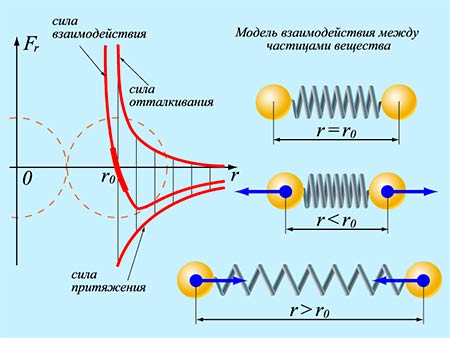
Malunok 3 . 1 . 2 znázorňujúce akumuláciu výslednej sily F a potenciálnu energiu interakcie medzi molekulami spomedzi centier. Pri vіdstanі r = r 0 sa sila interakcie zmení na nulu. Je chytro akceptovaný ako priemer molekuly. Keď r = r 0, potenciál energie v spojení s modalitou je minimálny.
Obchodná hodnota 6
Keď sú dve molekuly zozadu r 0 vedľa seba E 0 energizuyu zvyazyu chi s glybínovými potenciálmi.

Malunok 3. 1. 2.Sila interakcie Fže potenciálna energia interakcie E p dve molekuly. F> 0- Sila priťahovania, F< 0 - sila ťažkého.
Fragmenty molekúl môžu mať malú veľkosť, ale jednoduché monatomické môžu byť väčšie ako 10 - 10 m.
Obchodná hodnota 7
Ja nazývam pustý chaotický výsmech molekúl tepelný odpad.
Keď teplota stúpa, kinetická energia tepelného kolapsu sa zvyšuje. Pri nízkych teplotách sa priemerná kinetická energia spravidla javí ako nižšia hodnota pre hodnotu glybínového potenciálu E 0. Dánsko ukazuje, ako molekuly pretekajú zo stredu alebo zo stredu medzi nimi r 0. Keď teplota stúpa, priemerná kinetická energia molekuly sa mení E 0, pretože zápach rastie a vytvára reč podobnú plynu.
V pevných telesách sa molekuly hladko zrútia s pevnými stredmi, takže poloha je rovnaká. V priestore môže byť nepravidelné usporiadanie (v amorfnom til), alebo v dôsledku zavedeného usporiadania veľkých štruktúr (kryštalický til).
Agregátne stanice Rechovín
Voľnosť tepelného kolapsu molekúl vidieť v hrebeňoch, pretože nemajú žiadne väzby na stredy, takže umožňujú posun v celom objeme. Tsim vám vysvetlí її plinness.
Obchodná hodnota 8
Len čo sa molekuly priblížia, môžu určiť poradie štruktúry s množstvom molekúl. Pomenujem vystúpenia pre Dana uzavrieť objednávku. Vzdialený poriadok charakteristické pre kryštalické til.
Pozrite sa na plyny s molekulami a ďalšie doyuchі hlúpe malý, keď ruchi ide von rovno, skontrolujte zámok. Hodnota je 10-8 m є priemerná veľkosť molekúl prášku v normálnych mysliach. Oskіlki vzamodіya sily sú slabé, plyny expandujú a môžu zapovnyuvat byť ako objem rozsudku. Ak interakcia їхnya nie je nulová, potom hovorte o prejave ideálneho plynu.
Kinetický model ideálneho plynu
V mkt sa počet reči podieľa na proporcionálnom počte častíc.
Obchodná hodnota 9
Mil- Celý počet slov, ako sa pomstiť časticiam častíc (molekúl), aby sa odohral v 0,012 kg atómov uhlíka C 12. Molekula uhlíka sa skladá z jedného atómu. Znie to ako nápoj, ale 1 mol reči stojí za rovnaký počet molekúl. Číslo, na ktoré sa má volať post_noyu Avogadro NA: NA = 6, 02 ċ 1023 mol - 1.
Vzorec pre hodnotu počtu reči ν zapísať do množiny N počtu častíc na poste Avogadra N A: = N N A.
Obchodná hodnota 10
Masoyu jedna modlitebná reč Molárnu hmotnosť nazývam M. Vaughn sa prilepí na diváka vzorca M = N А ċ m 0.
Viraz molárnej hmotnosti sa vykonáva v kilogramoch na mol (na g / mol).
Obchodná hodnota 11
Pokiaľ ide o reč, sklad má jeden atóm, takže je ľahké hovoriť o atómovej hmotnosti dielu. Jednotka atómu - hmotnostný izotop tse 1 12 v uhlíku C 12 sa nazýva atómová jednotka prihlasujem jaka ( a. jesť.): 1a. e. m. = 1, 66 ċ 10 - 27 pred Kr
Hodnota je uvedená pre hmotnosť protónu a neutrónu.
Obchodná hodnota 12
Hmotnosť atómu, ale molekúl danej reči do 1 12 hmotnosti atómu v uhlíku je tzv. obdivuhodný masoyu.
Yaksho Vi označili v texte odpustenie, buď lasička, pozri a natisnit Ctrl + Enter
Až donedávna boli stanovené základné princípy molekulárno-kinetickej teórie (MKT) Budova a reči. Hmotnosť a veľkosť molekúl. Postiyna Avogadro.Molekulárno-kinetická teória je reťazec fyziky, ktorý je zodpovedný za silu starých rečových stavov a ako vysvetliť javy o objavovaní molekúl a atómov ako nájdených častí reči. IKT sú založené na troch základných ustanoveniach:
1. Usi reči sú uložené z nájdených častíc: molekúl, atómov a iónov.
2. Drobn castice prehlusuj nepreruen chaotick rus, ktorho rchlos je teplota prejavu.
3. Medzi malými časticami dochádza k ťažkému a ťažkému účinku, ktorého povaha leží v ich strede.
Hlavné ustanovenia IKT potvrdzujú ďalšie skutočnosti. Molekuly, atómy a ióny boli vychované experimentálne, molekuly boli odoberané a fotografované pomocou elektronických mikroskopov. Stav plynu nie je prepojený, aby expandoval a zaberal celú zásobu a dá sa vysvetliť neprerušovaným chaotickým kolapsom molekúl. Pružnosť plynov, pevných a tvrdých častíc, sila slabosti pevnej látky, procesy farmárčenia, lepenia, konzervovania tvorby pevných povrchov a o sile ťažkých molekúl a energie sa dá veľa hovoriť. Fenomén difúzie – schopnosť molekúl tej istej reči prenikať na rozhraní s inými molekulami – podporuje aj hlavné tézy MCT. Prejav difúzie vysvetľuje napríklad rozširovanie pachov, zmenu vývoja rôznych typov, proces rozhodovania pevných častíc na okrajoch, proces prerážania kovu spôsobom tavenia, alebo úchopom. . Na podporu neprerušovaného chaotického kolapsu molekúl є ako aj hnedastého rúna - neprerušovaného chaotického kolapsu mikroskopických častíc, nestráviteľných pri ridin.
Rukh hnedastých častíc sa vysvetľuje chaotickým drobením ridinových častíc, ktoré sa vkrádajú do mikroskopických častíc a nasmerujú ich na ruh. Mimochodom, bulo bolo informované, že frekvencia hnedastých častíc zostane pri teplote ridini. A. Einstein prelomil teóriu Brownovej rue. Vykonajte ruck častíc štatistického, imovirnіsnyho charakteru. Existuje len jeden spôsob, ako znížiť intenzitu hnedastého zákalu - zmeniť teplotu. Vzhľad hnedastého kormidla sa posúva na koniec molekúl.
Či už je reč zložená z častíc, počet reči sa berie úmerne k proporcionálnemu počtu častíc, takže v miestnosti možno nájsť štrukturálne prvky.
Jeden počet slov je є krtek. Mole je celé číslo reči, teda pomstiť sa na štýle a štruktúrnych prvkoch či už ide o reč, alebo sa odohrávať v 12 g atómov v uhlíku C12. Pomer počtu molekúl reči k počtu molekúl reči sa nazýva Avogadrova postprodukcia:
Potom, čo Avogadro ukazuje, koľko atómov a molekúl možno nájsť v jednom mole reči. Molová hmotnosť je hmotnosť jedného mólu reči, čo je veľmi drahé pre množstvo reči k počtu reči:
Molárna hmotnosť sa uvádza v kg / mol. Keď poznáte molárnu hmotnosť, môžete vypočítať hmotnosť jednej molekuly:
Priemerná hmotnosť molekúl závisí od chemických metód, postprodukcia Avogadro s vysokou presnosťou je priradená fyzikálne metódy... Hmotnosť molekúl a atómov je významnou úrovňou presnosti, ktorá začína pomocou hmotnostného spektrografu.
Molekuly sú ešte menšie. Napríklad hmotnosť molekuly olova:
Molárna hmotnosť je viazaná na prípustnú molekulovú hmotnosť Mg. Typická molekulová hmotnosť je hodnota, ktorá je vysoko relevantná pre hmotnosť molekuly danej reči až do 1/12 hmotnosti atómu v uhlíku C12. Pokiaľ sa nájde chemický vzorec reči, potom, mimo Mendelovej tabuľky, môže byť označený ako špecifická hmotnosť, pretože pri otáčaní v kilogramoch ukáže hodnotu molárnej hmotnosti reči.
03.02.2015
Lekcia 39 (10. ročník)
Téma. Hlavné ustanovenia IKT Budov a prejavy a її donedávna
1. Vedenie kurzu molekulovej fyziky a MCT; makro a mikro
Uhádnime hŕstku všetkých častí fyziky v popredí, ktoré sme videli, a vizuálu, že sme sa celé hodiny pozerali na procesy, ktoré sme sledovali pomocou makroskopických objektov (alebo makier). Teraz budeme môcť vidieť procesy, ktoré prebiehajú uprostred nich.
Viznachennya. Makroskopické tilo- Tilo, ako uskladniť veľké množstvo častíc. Napríklad: auto, lyudin, planéta, biliard kul ...
mikroskopické tilo - tilo, je možné skladovať z jednej alebo niekoľkých častíc. Aplikácia: atóm, molekula, elektrón ... (obr. 1)

Malý. 1. Použite mikro-makro-objekt ako príklad
Po pomenovaní predmetu IKT kurzu v takomto poradí potom hovorte o hlavných cieľoch, ako nastaviť kurz IKT pred vami a o sebe:
1. Vivchennya procesy, ktoré sa vykonávajú uprostred makroskopického objektu (proces vzájomného spojenia častíc)
2. Výkon výkonu (výkon, hmotnosť, zverák (na plyn) ...)
3. Vivchennya tepelných prejavov (kúrenie-chladenie, zmeny agregátových staníc)
Výživa Vivchennya tsikh, pretože prechádza napínavým úsilím tých, ktorí vyrastú v rovnakom čase z toho, čo formulujem takzvané základné ustanovenia IKT, takže pravdou je, že je to už dávno, čo celá budúcnosť
Postarajte sa o to mimochodom:
2. Perche je hlavným táborom MKT; molekuly, atómy
Úsilie hovoriť sa skladá z veľkého počtu častíc - molekúl a atómov.
Viznachennya. atóm- Našiel som časť chemického prvku. Veľkosť atómov (їх priemer) je rádom božského. odlišné typy atóm, pokiaľ ide o molekuly, zjavne nie je veľký. Ľudia bez námahy, ako napríklad tohtoroční, vyberaní z takzvanej mendelovskej tabuľky (oddiel obr. 2)

Malý. 2. Periodická tabuľka chemické prvky(podľa dňa typu atómov) D. I. Mendeleva
Molekula- Je to štrukturálna jednotka reči, ktorá môže byť uložená z atómov. Pri pohľade na atómy je vôňa skvelá a dôležitá pre zvyšok a smola, vôňa môže byť veľkou všestrannosťou.
Rieka, molekula, ktorá sa skladá z jedného atómu, sa nazýva atómový, s veľké číslo – molekulárne... Napríklad: bozk, voda, kuchynské jedlo() - molekulárny; héliové médium (He, Ag) - atómové. 
Navyše vďaka inteligencii nebude sila makroskopických predmetov ukrátená o niektoré vlastnosti mikroskopického skladu, ale o tie špecifickejšie.
Iakshho v Budove Atomiv Rechovina môže používať geometriu ( krištáľové zadarmo), pretože, no, navpaki, nie je, potom sa tsim tilam zapletie do moci. Napríklad amorfný prach neovplyvňuje teplotu topenia. Nayvidomish pažba - celý amorfný grafit a kryštalický diamant. Urážlivé slová sú uložené z atómov v uhlí.


Malý. 3. Napríklad grafit a diamant
S takouto hodnosťou "zi skilkoh, v ktorej recipročnej ružici takýchto atómov a molekúl je reč?" - prvá potrava, zdá sa, že nás približuje k pokoju autorít tiel.
3. Ďalšia hlavná stanica MKT
Používajú malé časti opúšťajúce neprerušovaný tepelný chaotický rus.
Takže je to, ako v zadkoch, že na pohľad je viac dôležitejšie ako najmenšie aspekty ruky, ale o to dôležitejšie pre nové slová.
Molekuly a atómy pevných látok sú zbavené malého množstva času z ich vlastného stacionárneho tábora; ridkikh - ide tiež o potrasenie si rúk, pivo cez veľké dimenzie molekulárneho priestoru, jeden po druhom; častice plynu, vlastné prúdy, nie sú veľmi zaneprázdnené, môžu sa ľahko pohybovať po voľnom priestranstve.
4. Tretia základná pozícia MKT
Častice vzaєmod_yut jedna s jednou.
Interakcia je elektromagnetickej povahy (interakcia jadier a elektrónov atómu) a oboje na útočnej strane (obe sú priťahované, tak aj priťahované).
Tu: d- Objaviť sa medzi kusmi; a- Veľkosť častíc (priemer).

„Atóm“ prvýkrát predstavil starogrécky filozof a prírodovedec Demokrot (obr. 4). V poslednom období aktívne dodávajú výživu o štruktúre mikroruského učenia Lomonosova (obr. 5).


Malý. 4. demokrat Mal. 5. Lomonosov
5. Rіznі možnosti pre obruntuvannya pozíciu MKT
V prípade klasu je hlavná poloha MCT uhádnutá, ale samotná:
1. Úsilie sa skladá z malých častíc - molekúl a atómov,
2. Tsі častice perebayut v post-chaotickom Rusі,
3. Tsi časti bez pererervno výmeny medzi sebou.
Ako teda opraviť potvrdenie potvrdenia? Kvôli jednému zo spôsobov, ako poznať kožu bez viny, Lyudin. Tse difúzie, pre zmіshuvannya, hovoriť jednoduchým jazykom.
Viznachennya. Difúzia- proces vzájomného prenikania molekúl tej istej reči v priestore medzi molekulami mysle (obr. 6).

Malý. 6. Proces difúzie v plynoch
Difúziu možno nájsť v plynoch (môžeme podporiť proces a je vidieť rozšírenie pachov), v rіdinoch (zmena nasiaknutej vody a starých farieb) a hladkú v tvrdých húževnatých, často budú rozpoznané iba tri listy, jeden arkuš bude koniec a jeden bude opravený). Navyše dochádza aj k zmene difúzie, takže molekuly plynu prenikajú do tuhej látky a tuhej látky (riba vo vode nemohla žiť) tenko (obr. 7).


Malý. 7.rôzna difúzia zadku
Je pravda, že ak to necháte tak, ale reč je jedinečná, podozrivá štruktúra, vek je nerozumný, pretože vysvetľuje dôvody prejavu.
Protestujte proti hlavnému argumentu objasnenia hlavných ustanovení IKT є Brownian ruh.
6. Popis Brownovej rady
Viznachennya. Brounivskyi rukh- neprerušovaný tepelný chaotický tok molekúl reči (obr. 8).
Tsey termín uzvichayvsya za to, yak na 1827 p. Škótsky botanik Robert Brown, prevracajúci plavákové súbory vo vode a hľadiaci na škvrnu šialenstva pod mikroskopom, vyvolávajúci odhady ruhu.

Malý. 8. Traktorіya malej časti v Brounivskiy Rusі
7. Objasnenie podľa Brownovej rady
Brownove úlomky sa však mohli pozrieť na súbor v mikroskope bez častice pilníka, pretože nesprávne interpretoval svoje videnie (mysliac si, že súbor je živý). Brownovu ploticu je možné vysvetliť na základe molekulárno-kinetickej teórie.
Dôvod hnedastého žmolku častice paseky je ten, že vplyv molekúl redinu na časticu nekompenzuje jednu vec..
Na malej 8.4 je schematicky znázornená poloha jednej hnedej časti molekúl, ktorá je k nej najbližšie. V prípade chladných rus molekúl sa prenesú do hnedastej časti impulzu, napríklad ruka a pravá ruka nie sú rovnaké. Je to kvôli nulovej výslednej sile zovretia nodulárnych molekúl zo strany hnedých. Qia moc a wiklikak do skazy časti.
 Malý. 9. Brounivska časť súboru pri vode
Malý. 9. Brounivska časť súboru pri vode
Stredný grip je pre plyn menej výrazný, rovnako ako pre ridini. Ak vidíte nevýznamné správy z priemernej hodnoty. Chim menšie povrch podlahy, ktorý sa oslabil o viznі vіnіnі, stlačil zverák, tak ďalej na celú oblasť. Ak teda napríklad majdan narástol do rádu decilových priemerov molekuly, tak sila zovretia, ktorá na ňom pôsobí, sa zmení z nuly na určitú hodnotu, keď sa molekula dostane do celého majdanu.
Pobudov teórie Brownovho ruchu a experimentálna podpora francúzskeho fyzika J. Perrina dokončila modifikáciu molekulárno-kinetickej teórie. Nemecký fyzik Albert Einstein (1879-1955) ešte v minulom storočí videl, že veľký kus pilníka jednoducho nahodili lopatou na množstvo iných molekúl vody, pretože samy sa chaoticky zrútili (Mal. 9).
O niečo viac opatrnosti sa dá dosiahnuť tými najjednoduchšími spôsobmi: zhoďte čelovku blízko vody a pozrite sa na vrchol pod mikroskopom, skúste držať krok s práškom, ako sa vám zrúti v byte.
8. Dôkaz základov
V takejto hodnosti prejav hnedastej rue zvýši prijatie zavádzania IKT. Samotný fakt súboru je pidtverzhu їkh. Súbory Yakshcho sa zrútili, to znamená, na novú silu. Na zámenu síl je len jeden dôvod – fixácia malých til. Otzhe, už neuvážene, na prvých dvoch pozíciách. Kmity súboru sa menia priamo, aj v momente hodiny je množstvo úderov na súbor zo speváckej strany toho druhého;
Hnedastý rox je tepelný rox a nedá sa na ňom zavesiť. Pri vyšších teplotách intenzita rastu. Diagram ruch Brownových častíc ukazuje na 8,3. Poloha častíc, označená bodkami, označená v rovnakých intervaloch hodiny - 30 s. Tsi body z'єднані priamok. Pre traktorіya malých kúskov nabagato skladnіsha.
Brownian Rukh môže byť hostený plynom. Yogo zd_yisnyuut zazhenі pri každej častice videl chi dima. Barvysto opisuje Brownov ruh od nimetského fyzika R. Paula (1884-1976): „Existuje veľa vecí, na ktoré sa môžete tešiť, ako napríklad ruh na sušienky. Tu je sposterіgachevі dovolené pozerať sa za lashtunks

okrem toho vidieť prírodu. Pred ním vidieť Nový Svit- bezúhonná metušna majestátneho množstva častíc. Shvidko rozliať v zornom poli mikroskopu nájdené častice, mayzhe mittєvo zmiyuyuchi rovno na zem. Viac čiastočiek kvapká stále viac a viac, smrad sa postupne sťahuje rovno k zemi. Veľké časti sú praktické na premiestňovanie doma. Їхні vo vzhľade jasne ukazuje obalenie častíc okolo svojej osi, pretože sa neustále mení priamo pred otvoreným priestorom. Nikde nie je poriadok systému. Panuvannya sl_pogo vipadku - os jaka je silnejšia, dôležitejšia ako nepriateľ, obrázok je zobrazený na plagáte. pontón Nini hnedastý rukh vikorystovuєtsya v širšom zmysle. Napríklad s hnedastým kolapsom є chvejúce sa šípky citlivých vimіryuvalnыh príloh, ktoré prechádzajú tepelnou suťou atómov detailov pripojených k tomu navkolishny stred.
Doslidi Perrin. Myšlienka Perrenových diapozitívov
Zdá sa, že koncentrácia molekúl v plyne atmosféry sa mení s výškou. Ak nedošlo k tepelnému kolapsu, potom všetky molekuly spadli na Zem a atmosféra sa prebudila b. Keďže to však nebolo pre Zem ťažké, potom by molekuly na tepelné úlomky boli spotrebované Zemou a fragmenty plynu by sa vytvárali na neobmedzenú expanziu. Spolu s radom ďalších faktorov vzniká ojedinelý rast molekúl, ako sa hovorí viac, takže koncentrácia molekúl sa môže rýchlo meniť s poklesom. Navyše, s väčšou hmotnosťou molekúl, tým rýchlejšia je zmena koncentrácie.
Hnedasté malé časti berú svoj osud z termálneho rusi. Takže keďže interakcia їхnya je dychtivo malá, potom množstvo cych častíc v plyne, alebo dokonca viac, možno považovať za ideálny plyn z ešte dôležitejších molekúl. Podľa tohto zákona sa mení aj koncentrácia hnedých častíc v plyne pôvodu v poli zemskej príťažlivosti, ako koncentrácia molekúl plynu. Zákon Vidomy.
Perrin za pomoci mikroskopu veľkého malý glibini Polia zoru (trochu vlnky) sú v hnedastých častiach ušetrené ešte tenšie guľôčky ridini. Koncentrácia častíc v nižších výškach je zvýšená koncentráciou častíc v nižších výškach a koncentrácia častíc je znížená samotným zákonom a koncentráciou molekúl v plyne. Zdá sa mi, že pre veľkú hmotnosť Brownových častíc je pokles viditeľný ešte rýchlejšie.
Navyše, podrakhunok hnedých častíc v nižších výškach, čo Perrinovi umožňuje oceniť post-Avogadro novou metódou. Význam procesu trvalej straty z videnia.
Všetky fakty svedčia o správnosti teórie Brownovej skazy a zrejme aj o tom, že Brownove časti sa zúčastňujú tepelnej fázy molekúl.
