Moč ozona, njegov odnos z razvojem govora in področjem shranjevanja. Nadzor ozona v vodi Nadzor ozona v vodi
OZON (O 3) je alotropna sprememba kislosti, molekula je zložena iz treh atomov v barvo in po možnosti iz vseh treh agregatnih mlinov. Molekula ozona ima strukturo v obliki rionsko-stegneničnega tricikla z vrhom 127 o. Vendar se zaprti tricikel ne uveljavi, ima pa molekula konoplje lantyuga 3 atome v obliki 0,224 nm. Odvisno od molekularne strukture je dipolni moment skladišča 0,55 debye. V elektronski strukturi so molekule ozona oštevilčene z 18 elektroni, ki tvorijo mezomerno stabilen sistem, ki se uporablja v drugih državah blizu Cordona. Prikordonnyjeve ionske strukture predstavljajo dipolni značaj molekule ozona in razlagajo njeno specifično reakcijsko vedenje v smislu kislega, ki je radikal z dvema neparnima elektronoma. Molekula ozona je sestavljena iz treh atomov. Kemična formula za plin -O 3 Reakcija na ozon: 3O 2 + 68 kcal / mol (285 kJ / mol) ⇄ 2O 3 Molekulska masa do ozona - 48 At sobna temperatura ozon je plin, ki se ne zadržuje in ima značilen vonj. Vonj ozona je zaznan pri koncentraciji 10 -7 M. V domači državi je ozon temno modre barve s temperaturo taljenja -192,50 C. Trdni ozon je kristal črne barve s temperaturo -111,9 stopinj C. Pri temperaturah 0 gr. і 1 atm = 101,3 kPa, koncentracija ozona postane 2,143 g / l. V plinastem mlinu je ozon diamagnetni in izpušča iz magnetnega polja, v plinskem mlinu je šibko paramagnetni, tako da je volodin. magnetno polje in se potegne v magnetno polje.
Kemija ozona
Molekula ozona je nehlapna in se pri normalnih umih pri zadostnih koncentracijah s pojavom toplote pretvori v dvoetažni kisik. Prilagoditev temperature in zmanjšanje tlaka za povečanje učinkovitosti porazdelitve ozona. Stik z ozonom v majhnih količinah organski govori, Kovine ali oksidi Deyakikh bodo hitro pospešili transformacijo. Kemična aktivnost ozona je še večja, vendar je močno oksidant. Vse kovine so bile oksidirane in vse so bile kovine (za vinatko iz zlata, platine in iridija) in veliko nekovin. Produkt reakcije je predvsem kissen. Ozon je mogoče najti v vodi bolj barvito, manj rožnato, brez zapletene raztopine, poleg tega pa je hitrost njegove porazdelitve v območju 5-8 krat v hrani, ne v plinski fazi, ne v plinski fazi (Rozumovskiy SD, 1990 ). Cena očitno ni posledica posebnosti kondenzirane faze, ampak zaradi reakcij s hišami in iona hidroksila; Razlika med ozonom in natrijevim kloridom je skladna s Henryjevim zakonom. S povečanjem koncentracije NaCl v sproščanju vode se stopnja sproščanja ozona zmanjšuje (Tarunina V. N. in spívavt., 1983). Ozon je še manj konkurenčen do elektrona (1,9 eV), ki je močno oksidacijsko sredstvo, ki je boljše od fluora (Rozumovskiy S.D., 1990).Biološka moč ozona in njegov vnos v človeško telo
Visoka oksidacijska zgradba in tisti, ki so v kemijskih reakcijah bagatokh, ki se zavzemajo za sodelovanje ozona, se pretvarjajo, da so kisli radikali, zajezitev celotnega plina na robu ni varna za ljudi. Jaku plin podoben ozon, vbrizgan na lyudin:- Dratu і poshkozhu tkanine iz organske dikhannye;
- Prelivanje holesterola v krvi človeka, zaznavanje nevronskih oblik, ki vodijo v aterosklerozo;
- Dovge znakhozhennya na sredini s povečano koncentracijo ozona je lahko razlog za cholovic bezpliddya.
- Največja dovoljena enkratna mejna dovoljena koncentracija (GDK m.r.) v atmosferska hrana populacija m_sc 0,16 mg / m 3
- Srednje podobna mejna dovoljena koncentracija (GDK d.s.) - 0,03 mg / m 3
- Mejna dovoljena koncentracija (HDC) v drugi delovni coni je 0,1 mg / m 3 (hkrati je čas vonja po človeku blizu 0,01 mg / m 3).
Visoka in nizka moč ozona
Ozon je prisoten v dveh sferah ozračja. Troposferski oz prizemni ozon, ki se nahaja v krogu atmosfere najbližje površini Zemlje, v troposferi ni varen. Zmagajte shkidliviy za ljudi in za druge žive organizme. Vino odvaja zobe na drevesih za gojenje svilnato raznolikih kultur. Poleg tega je troposferski ozon eden vodilnih "Ingredіntіv", ki jih lahko. Ob isti uri je stratosferski ozon celo cimet. Ruynuvannya, ki ga je nastavil ozonsko kroglo (ozonski zaslon) za proizvodnjo, preden tok ultravijolične viprominuvannye na zemeljsko površino naraste. Zaradi rasti številnih bolezni raka shkiri (vključno z najbolj nevarno vrsto melanoma) so se pojavile okužbe sive mrene. Injekcija trdega ultravijoličnega sevanja oslabi imuniteto. Pretirana izpostavljenost ultravijoličnemu sevanju je lahko tudi problem Silskoy vlada Torej, kako lahko naredite svoje pridelke tako občutljive na ultravijolično. Iste ure je spomin zdrsnil, scho ozon je odpadni plin in ob rivnu zemeljsko površino zmago bomo težko prizadeli. Pod vplivom intenzivne zaspane viprominuvannye in specifikacij na vsakem koraku se pretvarja, da je še posebej bogat s slastnim ozonom.Vzaêmodiya ozon in kisla ena za drugo. Podrobnosti in podrobnosti.
Ozon je alotropna oblika kisline. Alotropija je manifestacija enega in istega kemičnega elementa v dveh ali več preprostih besedah. V tem primeru sta odobrena ozon (O3) in kisik (O 2) drzen element O. Otrimannya do ozona iz kislosti Yak se praviloma za zavržek ozona uporablja molekularni kisik (O 2), sam postopek pa je opisan z običajnim 3O 2 → 2O 3. Reakcija je endotermna in zlahka reverzibilna. Za nadomestitev ravnovesja v celotnem izdelku (ozon) pridite. Eden od načinov za odpravo ozona je uporaba obloka. Toplotna disociacija molekul z naraščajočo temperaturo. Torej pri T = 3000K - zm_st atomske kislosti postane ~ 10%. Temperaturo v nekaj tisoč stopinjah je mogoče prilagoditi za dodaten lok. Vendar se pri visokih temperaturah ozon razvija hitreje kot molekularna kislost. Možno ga je znebiti, spremeniti, ogreti plin in nato hitro ohladiti. Ozon v tej obliki je vmesni produkt med prehodom iz vsote O 2 + O v molekularno kislino. Največja koncentracija O 3, jaku je mogoče obrezati s tem načinom proizvodnje, doseg je 1%. Povsem dovolj za številne industrijske namene. Moč oksidacije ozona Ozon je trdo stisnjeno oksidant, ki je bolj reaktiven v porozni kislini. Oksidacija vseh kovin in bogato nekovin v skladu z odobritvijo kislosti: 2 Cu 2+ (aq) + 2 H 3 O + (aq) + O 3 (g) → 2 Cu 3+ (aq) + 3 H 2 O (1) + O 2 (g) Ozon lahko igra vlogo pri reakcijah peči, temperaturi peči pri celotni temperaturi, nižji pri temperaturi v atmosferi dvoetaminske kisline: 3 C 4 N 2 + 4 O 3 → 12 CO + 3 N 2 Standardni potencial za ozon je 2,07 V, zato se molekula ozona ne spremeni in se pretvori v toploto v obliki toplote. Pri nizkih koncentracijah se ozon razvija pogosteje, pri visokih koncentracijah - z vibuhom, zato ima molekula odvečno energijo. Ogrevanje in stik z ozonom z majhnimi delci organskih tekočin (hidroksid, peroksid, kovina nizke valence in drugi oksidi) hitro pospešijo transformacijo. Navpaks, prisotnost majhnih količin dušikove kisline in stabilizira ozon ter v posodah iz skladišča in nekaterih plastičnih mas ali čistega kovina ozon pri -78 0 C. je praktično razpet. Konkurenčnost ozona za elektronska vrata 2 ev. Tako močna je spora volodina le fluor in oksid. Ozon je oksidiral vse kovine (za vinjeto iz zlata in platine), pa tudi veliko drugih elementov. Klor skrbi za vlogo pri reakcijah z ozonom in hipokloritom OCL. Reakcije na ozon z atomsko vodo so dzherel za nastanek hidroksilnih radikalov. Ozon ima največjo vsebnost vlage v območju UV pri povečanju 253,7 nm z molskim koeficientom izumrtja: E = 2900 Pri dani UV-fotometrični vrednosti koncentracije ozona hkrati z jodno-metrično titracijo sprejetega standardi. Kisen na podlagi ozona ne vstopi v reakcijo s KI.Stabilnost ozona in vode
Likvidnost porazdelitve ozona v razponu 5-8 krat v hrani, nižja v plinski fazi. Razgradnja ozona v vodi je 10 -krat večja, kislost nižja. Po podatkih prejšnjih avtorjev se vrednost učinkovitosti ozona v vodi giblje od 0,49 do 0,64 ml ozona / ml vode. V idealnih termodinamičnih mislih se je treba držati Henryjevega zakona, tako da je koncentracija plina, ki se razgradi, sorazmerna z njegovim delnim porokom. C S = B × d × Рi de: С S - koncentracija juhe v vodi; d - masni ozon; Pi - delni oprijem ozona; B - učinkovitost izračuna; Genrijevo določanje zakona o ozonu kot metastabilnem plinu je pametno. Padec ozona v plinski fazi je v delnem poroku. V vodnem središču obstajajo nekateri procesi, ki presegajo področje zakona Genrija. Gibs-Dukem-Margulesdujev zakon bo v idealnih mislih zamenjal novega. Praktično je sprejeto, da se razlika v ozonu v vodi spreminja z zmanjšanjem koncentracije ozona v srednjih tleh na koncentracijo ozona v plinski fazi: Z enakimi ponori v vodi iz pipe koncentracija ozona postane 13 mg / l, v dvojno destilirani vodi - 20 mg / l. Razlog za to je znaten padec ozona skozi zimske hiše v bližini pitne vode.Zmanjšanje ozona v obdobju ivírozpadu (t 1/2)
V vodnem središču ozon močno pade glede na kakovost vode, temperaturo in pH v sredini. Povečanje pH srednjih tal bo pospešilo padanje ozona in znižalo koncentracijo ozona v vodi. Podobni procesi se pojavljajo pri nastavljivi temperaturi. Obdobje padca ozona v destilirani vodi postane 10 let, v demineralizirani vodi - 80 quilinov; v destilirani vodi - 120 quilinov. Zdi se, da je porazdelitev ozona v vodi s postopkom zlaganja reakcij radikalnih kislin: Največja količina ozona v vodnem očesu se prepreči v 8-15 minutah. Po enem letu se bo v vrstnem redu pojavilo le nekaj radikalov. Med njimi smo našli hidroksilni radikal (OH ') (Staehelin G., 1985), zato je treba spoštovati zdravljenje ozonske vode v terapevtske namene. Nihanja v klinični praksi za poznavanje količine ozonirane vode in ozonovanih fizioloških sprememb smo izvedli oceno količine ozonovana v količini ozona v koncentraciji, saj je ta v razširjenosti vitaminov v medicini. Glavne metode analize so bile jodometrična titracija in intenzivnost kemiluminiscence iz mikrovezja, pritrjenega na biokemiluminometer BKhL-06 (Nižnji Novgorod) (Kontorshchikova K.N., Peretyaginov S.P., 1995). Pojav kemiluminiscence je povezan z reakcijami rekombinacije vilnih radikalov, ki nastanejo pri dajanju ozona v vodo. Pri vzorčenju 500 ml dvo-destilirane vode in mehurčkov ozonsko-kislega plina z koncentracijo ozona med 1000-1500 mcg / l in hitrim pretokom plina 1 l / h v odseku 20 čilinov se kemiluminiscenca vyvii 160 Poleg tega je pri dvojno destilirani vodi intenzivnost svetlobe izključno, v destilirani vodi pa ne. Toleranca na ozon v razmerjih NaCl je v skladu s Henryjevim zakonom, da se zaradi povečanja koncentracije soli zmanjša. Psihološke okvare smo zalili z ozonom s koncentracijo 400, 800 in 1000 μg / L z odsekom 15 kilinov. Globalna intenzivnost svetlobe (v mv) se je povečala zaradi naraščajoče koncentracije ozona. Trivialnost svitinnye postane 20 hilin. Cena je razložena z obsežno rekombinacijo močnih radikalov in rezultati gašenja svetlobe za manifestacijo fiziološkega razvoja hiš. Ne glede na visok oksidacijski potencial je ozon zelo selektiven, saj je obremenjen s polarnimi budnimi molekulami. Tiho reagirajte z ozonom pol ure, tako da lahko nadomestite subtilen zvok (-C = C-). Posledično so občutljive na ozon nenasičene maščobne kisline, aromatične aminokisline in peptidi, ostriž za vse SH-skupine. Izhaja iz podatkov Kregea (1953) (citirano po Vieban R. 1994), prvega produkta interakcije ozonskih molekul z biološkimi substrati - 1-3 dipolarnimi molekulami. Reakcija je glavna pri interakciji ozona z organskimi substrati pri pH< 7,4.
Озонолиз проходит в доли секунды. В растворах скорость этой реакции равна 105 г/моль·с. В первом акте реакции образуется пи-комплекс олефинов с озоном. Он относительно стабилен при температуре 140 0 С и затем превращается в первичный озонид (молозонид) 1,2,3-триоксалан. Другое возможное направление реакции — образование эпоксидных соединений.
Первичный озонид нестабилен и распадается с образованием карбоксильного соединения и карбонилоксида. В результате взаимодействия карбонилоксида с карбонильным соединением образуется биполярный ион, который затем превращается во вторичный озонид 1,2,3 — триоксалан. Последний при восстановлении распадается с образованием смеси 2-х карбонильных соединений, с дальнейшим образованием пероксида (I) и озонида (II).
Največja količina ozona v vodnem očesu se prepreči v 8-15 minutah. Po enem letu se bo v vrstnem redu pojavilo le nekaj radikalov. Med njimi smo našli hidroksilni radikal (OH ') (Staehelin G., 1985), zato je treba spoštovati zdravljenje ozonske vode v terapevtske namene. Nihanja v klinični praksi za poznavanje količine ozonirane vode in ozonovanih fizioloških sprememb smo izvedli oceno količine ozonovana v količini ozona v koncentraciji, saj je ta v razširjenosti vitaminov v medicini. Glavne metode analize so bile jodometrična titracija in intenzivnost kemiluminiscence iz mikrovezja, pritrjenega na biokemiluminometer BKhL-06 (Nižnji Novgorod) (Kontorshchikova K.N., Peretyaginov S.P., 1995). Pojav kemiluminiscence je povezan z reakcijami rekombinacije vilnih radikalov, ki nastanejo pri dajanju ozona v vodo. Pri vzorčenju 500 ml dvo-destilirane vode in mehurčkov ozonsko-kislega plina z koncentracijo ozona med 1000-1500 mcg / l in hitrim pretokom plina 1 l / h v odseku 20 čilinov se kemiluminiscenca vyvii 160 Poleg tega je pri dvojno destilirani vodi intenzivnost svetlobe izključno, v destilirani vodi pa ne. Toleranca na ozon v razmerjih NaCl je v skladu s Henryjevim zakonom, da se zaradi povečanja koncentracije soli zmanjša. Psihološke okvare smo zalili z ozonom s koncentracijo 400, 800 in 1000 μg / L z odsekom 15 kilinov. Globalna intenzivnost svetlobe (v mv) se je povečala zaradi naraščajoče koncentracije ozona. Trivialnost svitinnye postane 20 hilin. Cena je razložena z obsežno rekombinacijo močnih radikalov in rezultati gašenja svetlobe za manifestacijo fiziološkega razvoja hiš. Ne glede na visok oksidacijski potencial je ozon zelo selektiven, saj je obremenjen s polarnimi budnimi molekulami. Tiho reagirajte z ozonom pol ure, tako da lahko nadomestite subtilen zvok (-C = C-). Posledično so občutljive na ozon nenasičene maščobne kisline, aromatične aminokisline in peptidi, ostriž za vse SH-skupine. Izhaja iz podatkov Kregea (1953) (citirano po Vieban R. 1994), prvega produkta interakcije ozonskih molekul z biološkimi substrati - 1-3 dipolarnimi molekulami. Reakcija je glavna pri interakciji ozona z organskimi substrati pri pH< 7,4.
Озонолиз проходит в доли секунды. В растворах скорость этой реакции равна 105 г/моль·с. В первом акте реакции образуется пи-комплекс олефинов с озоном. Он относительно стабилен при температуре 140 0 С и затем превращается в первичный озонид (молозонид) 1,2,3-триоксалан. Другое возможное направление реакции — образование эпоксидных соединений.
Первичный озонид нестабилен и распадается с образованием карбоксильного соединения и карбонилоксида. В результате взаимодействия карбонилоксида с карбонильным соединением образуется биполярный ион, который затем превращается во вторичный озонид 1,2,3 — триоксалан. Последний при восстановлении распадается с образованием смеси 2-х карбонильных соединений, с дальнейшим образованием пероксида (I) и озонида (II).
 Ozoniranje aromatskih spojin proti trditvam polimernih ozonidov. Uporaba ozona bo oslabila aromatično energijo v jedru in energijo vitrata, zato je učinkovitost ozonskih homologov glavni razlog za proizvodnjo energije. Ozonuvannya posušenih v ogljikovih hidratih je vezana na mehanizem vprovadzhennya. Ozonuvannya siro in dušik mešani organski spoluk na naslednji način:
Ozoniranje aromatskih spojin proti trditvam polimernih ozonidov. Uporaba ozona bo oslabila aromatično energijo v jedru in energijo vitrata, zato je učinkovitost ozonskih homologov glavni razlog za proizvodnjo energije. Ozonuvannya posušenih v ogljikovih hidratih je vezana na mehanizem vprovadzhennya. Ozonuvannya siro in dušik mešani organski spoluk na naslednji način:  Ozonídi zazvychay grdo razchinyayutsya v vodi, žal, v organskih razchinniki. Pri segrevanju nekatere prehodne kovine padejo v radikale. Število ozonidov v organski obliki je jodno število. Jodno število - masa joda v gramih, ki je bila dodana 100 g organskega govora. Za maščobne kisline jodno število ne sme biti 100-400, za trdne maščobe 35-85, za trde maščobe-150-200. Naprej ozon, kot antiseptik prvič A. Wolff leta 1915, prvi čas dneva. Prihajajoča usoda je korak za korakom zbirala podatke o uspešnosti uživanja ozona v primerih nedovoljenih bolezni. Vendar so bili vikoristi za trivialno uro prikrajšani za metodo ozonoterapije, povezano z neposrednimi stiki z ozonom s površin zvonjenja in tankih praznih prostorov. Zanima me ozonska terapija, saj sem v svetu videl kopičenje podatkov o biološkem učinku ozona na telo, imeli pa boste priložnost slišati o uspešnosti testiranja ozona v primeru cele vrste bolezni. Zgodovina medicinsko oskrbo ozon se popravlja od 19. stoletja. Pionirji klasične oskrbe z ozonom v zahodni Ameriki in Evropi, zokrem, C. J. Kenworthy, B. Lust, I. Aberhart, E. Payer, E. A. Fisch, N. N. Wolff in інši. Rusija ima zelo malo porabe ozona. Tilki v 60-70 letih v zadnjih letih literature iz široke uporabe razširjene metode razvoja ozonske terapije in o porabi ozona pri populaciji majhnih otrok v regiji ter v 80. letih v zgodovini našega Osnove za temeljni razvoj tehnologij ozonske terapije so v obliki robotov precej bogate na Inštitutu za kemijsko fiziko Akademije medicinskih znanosti ZSSR. Knjiga "Reakcije ozona in joga z organskimi govori" (SD Rozumovskiy, G. Ye. Zaikov, Moskva, 1974) je postala referenčna točka za razvoj mehanizmov za gospodarski razvoj ozona pri bagatih. Mednarodno ozonsko združenje (IOA) ima široko paleto dejavnosti, ki je imelo 20 mednarodnih kongresov, od leta 1991 pa so se naši zdravniki in znanstveniki udeleževali robotskih kongresov. Pozivamo na nov način, da pogledamo probleme uporabljenega zdravljenja z ozonom in v sami medicini. V terapevtskem območju koncentracij in odmerkov ozona je moč bioregulatorja s potiskom, ki je glede na metode tradicionalne medicine precej obilen in najpogosteje v obliki monoterapije. Zdravilni ozon Zasosuvannya je očitno novost aktualnih težav pri razvoju zdravstvenih težav. Tehnologije ozonske terapije se uporabljajo za zdravljenje v kirurgiji, porodništvu in ginekologiji, zobozdravstvu, nevrologiji s terapevtsko patologijo, nalezljivimi boleznimi, dermatologijo in spolnimi boleznimi ter številnimi drugimi. Ozonoterapijo odlikujejo preprostost, učinkovitost, dobra toleranca, praktična prepoznavnost stranskih učinkov, ekonomsko upravičena. Likuvalna moč ozona v primeru bolezni edinstvena stavba vlivati na organizm. Ozon v terapevtskih odmerkih za imunomodulatorne, antipiretične, baktericidne, proti kožnim, fungicidnim, citostatičnim, antistresnim in analgetičnim sredstvom. Yogo zdatnist aktivno popravlja škodo kisnevy homeostaze v telesu, ima velike možnosti za intravensko medicino. Širok spekter metodičnih možnosti omogoča zaradi velike učinkovitosti vikoristovuvati moč ozona za mišično in sistemsko terapijo. V zadnjih desetih letih so prišle do izraza metode, povezane s parenteralnimi (notranjimi, notranjimi, notranjimi, notranjimi) uvedenimi terapevtskimi odmerki ozona, aktivnimi sistemskimi učinki Kisnevo -ozonska plinasta vsota z visokimi (4000 - 8000 μg / l) koncentracijami v nizkem ozonu je učinkovita v primeru hudo vnetih, umazanih ran, gangrene, razjede na dekubitusu, diagnoz, glivičnih okužb šole itd. Ozon v visokih koncentracijah se lahko uporablja tudi kot krvno podprt. Nizka koncentracija ozona spodbuja popravilo, energetsko učinkovitost in vžig. Pri nekaterih kolitisih, proktitisih, noritih in pri številnih drugih črevesnih težavah je rektalno dajanje kislinsko-ozonskih plinskih vsot rektalno. Ozon, glede na fiziološko razčlenitev, med peritonitisom uspešno stagnira za sanacijo črnih odpadkov, ozonizirana voda pa se destilira v režni operaciji in v. Za notranjo uvedbo ozona vikorisovutsya, razchinny in fiziološke razchini abo v krvi bolne osebe. Pionirji evropske šole so sledili postulatu o tistih, ki z ozonoterapijo je: "Stimulacija in reaktivacija presnove kislin, ne da bi pri tem motili oksidativno -aktivne sisteme", - to pomeni, da se ob jemanju odmerkov na sejo tečaj. Riling, R. FIBA 1996 v knjigi. Ozonska terapija). V tuji medicinski praksi za parenteralno dajanje ozona vikoristovuyutsya, v glavnem, velika in majhna avtohemoterapija. Med veliko avtohemoterapijo so bolniku odvzeli streho, da se je znebil mešanice plinov kisik-ozon, in takoj kapljali nazaj v veno istega bolnika. Z malo avtohemoterapije se ozonirana streha vnese znotraj. Terapevtski odmerek ozona v celotnem razponu je prikazan za mešanico plina in koncentracijo ozona v novem.
Ozonídi zazvychay grdo razchinyayutsya v vodi, žal, v organskih razchinniki. Pri segrevanju nekatere prehodne kovine padejo v radikale. Število ozonidov v organski obliki je jodno število. Jodno število - masa joda v gramih, ki je bila dodana 100 g organskega govora. Za maščobne kisline jodno število ne sme biti 100-400, za trdne maščobe 35-85, za trde maščobe-150-200. Naprej ozon, kot antiseptik prvič A. Wolff leta 1915, prvi čas dneva. Prihajajoča usoda je korak za korakom zbirala podatke o uspešnosti uživanja ozona v primerih nedovoljenih bolezni. Vendar so bili vikoristi za trivialno uro prikrajšani za metodo ozonoterapije, povezano z neposrednimi stiki z ozonom s površin zvonjenja in tankih praznih prostorov. Zanima me ozonska terapija, saj sem v svetu videl kopičenje podatkov o biološkem učinku ozona na telo, imeli pa boste priložnost slišati o uspešnosti testiranja ozona v primeru cele vrste bolezni. Zgodovina medicinsko oskrbo ozon se popravlja od 19. stoletja. Pionirji klasične oskrbe z ozonom v zahodni Ameriki in Evropi, zokrem, C. J. Kenworthy, B. Lust, I. Aberhart, E. Payer, E. A. Fisch, N. N. Wolff in інši. Rusija ima zelo malo porabe ozona. Tilki v 60-70 letih v zadnjih letih literature iz široke uporabe razširjene metode razvoja ozonske terapije in o porabi ozona pri populaciji majhnih otrok v regiji ter v 80. letih v zgodovini našega Osnove za temeljni razvoj tehnologij ozonske terapije so v obliki robotov precej bogate na Inštitutu za kemijsko fiziko Akademije medicinskih znanosti ZSSR. Knjiga "Reakcije ozona in joga z organskimi govori" (SD Rozumovskiy, G. Ye. Zaikov, Moskva, 1974) je postala referenčna točka za razvoj mehanizmov za gospodarski razvoj ozona pri bagatih. Mednarodno ozonsko združenje (IOA) ima široko paleto dejavnosti, ki je imelo 20 mednarodnih kongresov, od leta 1991 pa so se naši zdravniki in znanstveniki udeleževali robotskih kongresov. Pozivamo na nov način, da pogledamo probleme uporabljenega zdravljenja z ozonom in v sami medicini. V terapevtskem območju koncentracij in odmerkov ozona je moč bioregulatorja s potiskom, ki je glede na metode tradicionalne medicine precej obilen in najpogosteje v obliki monoterapije. Zdravilni ozon Zasosuvannya je očitno novost aktualnih težav pri razvoju zdravstvenih težav. Tehnologije ozonske terapije se uporabljajo za zdravljenje v kirurgiji, porodništvu in ginekologiji, zobozdravstvu, nevrologiji s terapevtsko patologijo, nalezljivimi boleznimi, dermatologijo in spolnimi boleznimi ter številnimi drugimi. Ozonoterapijo odlikujejo preprostost, učinkovitost, dobra toleranca, praktična prepoznavnost stranskih učinkov, ekonomsko upravičena. Likuvalna moč ozona v primeru bolezni edinstvena stavba vlivati na organizm. Ozon v terapevtskih odmerkih za imunomodulatorne, antipiretične, baktericidne, proti kožnim, fungicidnim, citostatičnim, antistresnim in analgetičnim sredstvom. Yogo zdatnist aktivno popravlja škodo kisnevy homeostaze v telesu, ima velike možnosti za intravensko medicino. Širok spekter metodičnih možnosti omogoča zaradi velike učinkovitosti vikoristovuvati moč ozona za mišično in sistemsko terapijo. V zadnjih desetih letih so prišle do izraza metode, povezane s parenteralnimi (notranjimi, notranjimi, notranjimi, notranjimi) uvedenimi terapevtskimi odmerki ozona, aktivnimi sistemskimi učinki Kisnevo -ozonska plinasta vsota z visokimi (4000 - 8000 μg / l) koncentracijami v nizkem ozonu je učinkovita v primeru hudo vnetih, umazanih ran, gangrene, razjede na dekubitusu, diagnoz, glivičnih okužb šole itd. Ozon v visokih koncentracijah se lahko uporablja tudi kot krvno podprt. Nizka koncentracija ozona spodbuja popravilo, energetsko učinkovitost in vžig. Pri nekaterih kolitisih, proktitisih, noritih in pri številnih drugih črevesnih težavah je rektalno dajanje kislinsko-ozonskih plinskih vsot rektalno. Ozon, glede na fiziološko razčlenitev, med peritonitisom uspešno stagnira za sanacijo črnih odpadkov, ozonizirana voda pa se destilira v režni operaciji in v. Za notranjo uvedbo ozona vikorisovutsya, razchinny in fiziološke razchini abo v krvi bolne osebe. Pionirji evropske šole so sledili postulatu o tistih, ki z ozonoterapijo je: "Stimulacija in reaktivacija presnove kislin, ne da bi pri tem motili oksidativno -aktivne sisteme", - to pomeni, da se ob jemanju odmerkov na sejo tečaj. Riling, R. FIBA 1996 v knjigi. Ozonska terapija). V tuji medicinski praksi za parenteralno dajanje ozona vikoristovuyutsya, v glavnem, velika in majhna avtohemoterapija. Med veliko avtohemoterapijo so bolniku odvzeli streho, da se je znebil mešanice plinov kisik-ozon, in takoj kapljali nazaj v veno istega bolnika. Z malo avtohemoterapije se ozonirana streha vnese znotraj. Terapevtski odmerek ozona v celotnem razponu je prikazan za mešanico plina in koncentracijo ozona v novem. Znanstvene dosežke vikarjev so začeli redno posodabljati na mednarodnih kongresih in simpozijih
- 1991 - Kuba, Havana,
- 1993 - ZDA San Francisco,
- 1995 - FranziaLill,
- 1997 rock - Japonska, Kjoto,
- 1998 - Avstrija, Salzburg,
- 1999 r. - Nimechchina, Baden-Baden,
- 2001 - Anglija, London,
- 2005 - Francija, Strasbourg,
- 2009 - Japonska, Kjoto,
- 2010 rock - Španija, Madrid
- 2011 Turčija (Istanbul), Francija (Pariz), Mehika (Cancun)
- 2012r. - Španija Madrid
Vseslovenske znanstvene in praktične konference z mednarodno ozonoterapijo
I - "OZON V BIOLOGISU TA MEDICINI" - 1992 r., N.Novgorod II - "OZON V BIOLOGISU TA MEDICINI" - 1995 r., N.Novgorod III - "OZONE I UČINKOVITE METODE TERAPIJE" - 1998 r., N.Novgorod IV - "OZONE I UČINKOVITE METODE TERAPIJE" - 2000 RUR., N.Novgorod V - "OZON V BIOLOGISU TA MEDICINI" - 2003 r., N.Novgorod VI - "OZON V BIOLOGISU TA MEDICINI" - 2005 r., N.Novgorod"I Konferenca ozonske terapije Azijsko -Evropske unije ozonskih terapevtov in zdravstvenega zdravja" - 2006 r., Velikie Boldino, regija Nižnji Novgorod VII - "OZON V BIOLOGISU TA MEDICINI" - 2007 r., N.Novgorod U111 – "Ozon, aktivne formulacije in metode intenzivne terapije v medicini" - 2009 N. Novgorod Do leta 2000 je Ruska šola za ozonoterapijo oblikovala svojo obliko, evropsko, vse do vzpostavitve ozona kot preokupacije. Glavni razlog je širše izboljšanje fiziološkega odmerka v dozi ozona, zmanjšanje bistveno nižjih koncentracij in odmerkov ozona, razdrobljenost tehnologije zunajtelesne obdelave velikih koncentracij kisika v krvi (predelava ozona) V primeru največjih ruskih zdravnikov najučinkovitejše koncentracije ozona vedo, da osnovno načelo medicine »ni naše«. Varnost in učinkovitost ruskih metod ozonske terapije je bagatorazovogo pripravila in 100 -odstotno pripeljala do razvoja področja medicine. Kot rezultat osnovnih temeljnih kliničnih odmerkov znanstvenikov iz Bule iz Nižnjega Novgoroda je bila "Neizogibna pravilnost oblikovanja prilagoditvenih mehanizmov v organizmih delavcev s sistemsko infuzijo nizkih terapevtskih odmerkov ozona, ki sproži intenziviranje radikalnih reakcij , kar je posledično povečalo aktivnost encimskih in neencimskih lanokov antioksidativnega sistema za uničenje "(Kontorshchikova KN, Peretyagin SP)). Roboti vichiznykh so poznali razvoj nove tehnologije in vidik upravljanja z ozonom z naslednjo prednostjo:- Širok razpon kakovosti fiziološke vrtnice, razgrajene z ozonom (0,9% raztopina NaCl)
- Stagnacija sorazmerno majhnih koncentracij in odmerkov ozona med sistemsko infuzijo (intravaskularno in intraintestinalno dajanje)
- Infuzija notranjega ozoniranja
- Notranja koronarna uvedba ozonacije ni kardioplegična
- Popolno zunajtelesno zdravljenje z ozonom z veliko oskrbo s krvjo v primeru delnega krvnega obtoka
- Terapija z ozonom in kisikom z nizkim tokom
- Intraportalni vnos ozona
- Zasosuvannya ozon v gledališču
- Podporna sistemska ozonska terapija z biokemičnimi metodami nadzora
- Ozonska terapija je metoda brez zdravilne infuzije, ki omogoča odpravo pozitivnih rezultatov v primeru patologije geneze.
- Biološka aktivnost parenteralno danega ozona se kaže na ravni nizkih koncentracij in odmerkov, ki jih nadzirajo klinično spremenljivi pozitivni učinki zdravila, ki lahko očitno spreminjajo odmerek kopičenja.
- Obveščanje ruskih in evropskih šol o ozonoterapiji o tem, kako preučevati ozon v vlogi zdravnika, bo znatno izboljšalo učinkovitost terapije z zdravili, kar bo omogočilo zamenjavo zdravil v farmakologiji. Hkrati ozonska terapija uvaja močne kisle reakcije in procese obolelih organizmov.
- Tehnične zmogljivosti sodobnih medicinskih ozonatorjev z močjo ultra natančnega odmerjanja omogočajo uživanje ozona v območju nizkih terapevtskih koncentracij, podobnih tistim, ki se uporabljajo v farmakoloških pogojih.
7. Kje določiti potrebno uro čiščenja vode?
zdravje ozona ostanite pri vodi in ležite pri temperaturi
voda in območja stika plina z vodo.
Čim hladnejšo vodoі rosíkach manjše velikosti,
izračunalo se bo manj ozona. Chim vishche temperatura vode,
Tim shvidshe ozon pade na kislost in se porabi z viparovanny.
Padanje s stopnice tavajo naokoli
potrebna je vedno manjša koncentracija ozona.
8. Kaj je potrebno za dodatno filtriranje
voziti pislya ozonuvannya?
Voda Yakshcho je mystila veliko število
zapleteno s polovico, nato pa kot rezultat predelave
ozon v níy vipadaut rízní odpade.
Ta vrsta vode je potrebna dodatno filtriranje.
Za veliko filtriranja lahko izberete najpreprostejšo in
poceni filtri.
Z virom tsom njihovi roboti bodo dosegli pomemben napredek.
9. Chi slid se bati zapletene ure
zdravljenje z ozonom?
Vodi obdelava presežna količina ozona
Ne obremenjujte se z zobmi dediščine.
Plin se hitro spremeni v kissen,
Naslikal bom samo sijaj vode.
10. jasen pokazatelj kislosti vode,
opravil ozonuvannya?
voda maêšibka reakcija PH = 7,5 - 9,0.
11. Na skílshutsya vmest
kislo v vodi ozonuvannya?
vmist kisnyu v vodi bo trajalo 14 - 15 -krat.
12. Kako shvidko ozon pade v vodo?
V dvanajstih minutah po 10 minutah. koncentracija ozona se zmanjša
za polovico, pritrdi vodo in vodo.
Ob hladni vodi po 15-20 minutah. padec ozona
pol, pretvarjanje hidroksilna skupina in vodo.
13. Zakaj bi morali piti kislo vodo?
pidsilyu živi glukozo v tkivih in organih
zbílshu nasichuvanostі kisla krvna plazma
spremenite korak kisla lakota
barve mikrocirkulacija krvi.
nada pozitiven diyu
O presnovi jeter in niroku.
do robota srčno meso.
spremenite frekvenco dikhannya i
Zbilshu dichny obsyag.
14. Koliko potrebujete ozonuvat vode?
chim bolsh weanim hišna voda,
Tim je več kot eno uro obdelave.
Tako na primer ozoniranje 3 litrov oskrbe z vodo
posojilo 10 - 15 min
Pojdite na isto vožnjo vzeto iz voda,
med prazno med sezono, skala in podeželje
kriv se izvaja v tri-chotiri razi more.
15. Kdo ima lepše ozonuvati vodo v miscih ali kozarcu?
Jedi so lepše kot viberati Slišal bom zvok
grlo (kozarec) za povečanje koncentracije
ozona v medsebojno povezani družbi.
16. Če vodo za čaj lepše pobarvate,
do konca dneva?
Za kuhanje čaja voda ni priporočljiva
pripeljite do bistva.
Predenje t = 85-90 ° S.
Pred ogrevanjem opravite obdelavo vode.
17. Ali je možno ozonizirati mineralno vodo?
Takšne vode so na voljo vse minerale,
Čudovito in preperelo kislo.
Chi vas je počastil s statty?
Interakcija med ozonom in ozonom je odgovorna za neposredno reakcijo z ozonskimi molekulami ali celo z radikali, ki so v procesu kapljanja. Aktivnejši ozon v povezavi z anioni, nižji z nevtralnimi in kationskimi besedami.
Ozon, ki je aktivno oksidacijsko sredstvo, sodeluje z organskimi in anorganskimi besedami. S halogeni z ozonom ne reagira s fluorom in praktično ne vstopa v interakcijo s klorom. Brom oksidira z ozonom iz zmesi v hipobromit in nato v bromat ziednan. Hkrati se lahko vzpostavi bromid vzporedno z interakcijo organske aktivnosti z amiakom. Jod se z ozonom še bolj kakovostno oksidira in postane jodat in jodna kislina. Soli kislin, ki vsebujejo halogen, niso dovzetne za oksidacijo ozona. Praktično nevtralen do ozona je dušik in pol, vključno z amoniakom in amoniakom, pa tudi sam nitrat, s krivdo aminiva, prijazno medsebojno povezani s hidroksilnimi radikali. Strupene cianide zlahka oksidira ozon v cianidu, katerega nadaljnja oksidacija narašča še pogosteje in pospešuje le v prisotnosti ionov medija, da se spopade s prisotnostjo ionov v dolini. Voda in sulfati se v kombinaciji z ozonom oksidirajo v sulfate. No, če pride do reakcij s kovinami, potem ozon aktivno oksidira z oksidacijo galisa in mangana, kobalta in niklja, peroksidov in hidroksidov, kar lahko opazimo pri prekinitvi flokulacije ali filtracije. Krom je praktično pasiven do ozona;
"Članek Ozon za čiščenje vode... Govorili bomo o shranjevanju plina za bolj čisto vodo.
Ozon za čiščenje vode je tehnologija, ki se je spreminjala eno uro. Bilsh nízh del evropske zemlje vikoristovuyut ozonuvannya kot kratka metoda čiščenja vode. Francija je postala prva dežela, saj so ozon porabili s prečiščeno vodo.
Glavni razlog za ozon kot reagent pri čiščenju vode je dejstvo, da ni treba kupovati novih elementov, reagentov itd.
Ozon je kemično aktivna kemikalija, ki jo lahko shranimo iz treh atomov. Res je, da je tretji atom enostavno pripraviti in aktivno sodelovati z vašimi željami. Na splošno temelji tehnologija ozoniranja vode.
Ozon za razvoj naprednega reakcionarnega zdravja oksidira organske hiše, jih oropa z nepopravljivimi, jih poveča s takšnim uvrstitvijo, povečuje učinkovitost napadalnih korakov čiščenja vode.
Ozon oksidira v vodi, cinku, manganu, pomembni kovini, ga prevede v nekritičen mlin in leži dlje.
Prisotnost nesprejemljivih in glasnih vonjav. Takoj, ko je voda prisotna z vodo in amiakom, bo ozoniranje vode povečalo sproščanje teh besed.
Ozon nadaê chastkovo antinakípederavnoe díyu. Ozonuvannya vod in zaupanje v nastanek kalcijevih soli na stenah vročega cevovoda, in pogosto videli hladne usedline.
Sodobne tehnologije ozoniranja osebja deželnega osebja vse naredijo vse manj in manj. Oskilki učinek ozonuvannya kompleks, nato pa s prečiščeno vodo za celotne kabine v bližini bagatokh vipadkah, zlasti s "pomembno" vodo, lahko prenesete vključeno tehnologijo.
Zadnjica organiziranja čiščenja vode za dodaten ozon.
To ni recept za uporabo pri čiščenju vode, ampak je prikazan le na zadnjici, saj se lahko uporablja za ozoniranje pri pripravi vode.
Domnevno je stanje: čisto vodo je treba nadomestiti z 2,5 mg / l razbite fiziološke raztopine, stopnja oksidacije je 12 mgO2 / l, nesreča 5 mg / l, barva 30 stopinj. Tobto, voda je alamut, zelena, bogata z organskimi snovmi in lasmi. Chi ni dobra situacija, vanj se lahko prilega preprost odstranjevalec železa. Ale, res, mi zbiraêmosya zastosuvati mensh vitratne ozonuvannya.
Osnovno pravilo je, da mora biti odmerek ozona za čiščenje vode 0,14 *, ko je količina vode vidna, tako da se 0,14 pomnoži s koncentracijo vode. Dzherelo Žal mi je, da se ne spomnim. Naš odmerek ozona je 0,35 mg / l. Nihanje oksidacije je kompleksen kazalnik in v resnici ni mogoče biti tam, potem je odmerek ozona mogoče izčrpati le v praksi. Ozon v naši aplikaciji potrebuje 2 mg / l. Očitno je za 1000 litrov potrebnih 2000 miligramov ozona ali 2 grama. 1000 litrov - veliko vode, saj morate dodati 3-4 osebe.
Ozonatorji se razlikujejo glede na produktivnost: 1 g / leto, 2 g / leto, 4 g / leto itd. Pošlji več gramov za eno leto, dragi Tim. Res je, da je ozonizator vibriral za 1 g / leto. To pomeni, da traja 2 leti, da dobimo pogon za zadnjico. Kako bomo dobavili ozon? Še enostavneje je - žuboreti s kompresorjem v nabiralnem poka. Bulbashki, napolnjeni z ozonom, gredo skozi vodo, oksidirajo vse, kar se lahko oksidira, in počijo na površini vode. Ne vikoristany ozona je treba videti, tako da ozon dokonča otrobe. Za celoto do vhoda iz rezervoarja je nameščen filter z aktivnimi komponentami, kot je shranjevanje ozona. Vse je vredno dobrega prezračevanja.
Voda se dvigne, telo se poveča in že ga je mogoče filtrirati na začetni stopnji čiščenja vode, za dodatnimi izrednimi filtri mehanskega čiščenja tipa kartuše. Filtra ne bomo pogledali iz sredstev vugillama in dela industrijskega filtra. Ale tse je še vedno treba presenetiti za penije.
Potrebni so tudi ozonator s produktivnostjo 1 g / leto, rezervoar za 1000 litrov, kompresor za dovajanje ozonskih hranil v rezervoar, sistem za dovajanje ozona v rezervoar, grobi filter, črpalka pri postaja, filtri za čiščenje vode mehanike.
Shematično bo videti tako:

Otzhe, voda narašča iz zgornjega toka, da se zbere v Umnist. Raven vode in regulacija plovca do črpalke in elektromagnetnega ventila. Naenkrat se vklopite do časovnika, ki vam omogoča, da voznika pokličete le ponoči. Drugi časovnik vključuje ozonator in kompresor za dovajanje ozonsko-ozonske vsote v vodo. Programski časovnik za 2 leti robotov. Po dveh letih se ozonator in kompresor vključita.
Dve leti se ozon porablja v rezervoarju skozi cev z mozniki za enako oskrbo z ozonom po celotni prostornini rezervoarja. Zalizo oksidira, organske spojine oksidirajo, smrad se poveča in pade v obleganje.
Nato prtljaga vstane, odprite pipo - in črpališče tudi dovaja prečiščeno vodo skozi številne filtre (na primer 100 mikronov, valovite kartuše za 30 mikronov, kartuše za 5 mikronov in filtre)
Posledično voda ne zaseda mesta in je več kot organski govor.
Če želimo videti hiše, ki jih bomo povečali, bo trajalo le eno uro ozoniranja. Postopek poskusa preprostosti - v rezervoar so vlili vodo, 2 leti, leto, 3 leta, 4 leta so zamudili ozon in prilagodili videz vode.
Ne smemo pozabiti, da lahko ozon v vodi postaja vse bolj nepečen in bo za ljudi varen za 20, za vernosnost pa za 30 čilinov. Tobto, vodo lahko piješ šele čez celo uro.
Vazhaêmo ura: uho rezervoarja približno prvo leto noči. Polnjenje rezervoarja 2 leti - 3 leta. Ura za uničenje ozona v vodi - 30 quilinov. 3.30 noči - voda je pripravljena pred vikendom.
Vitrati na projektu minimalnih, od majhnih elementov - samo kartuš za mehansko čiščenje v srednji filtraciji, kot so kroglice ob prisotnosti kakršne koli sheme čiščenja vode - z ozonom in brez ozona. Drugi zimski elementi in vitratni materiali se ne uporabljajo - ne nadomeščajo katalitične konzervacije niti vitrata za mangan ali sil.
De ozonatori? V bistvu tiha podjetja, ki se ukvarjajo z bazeni. Smrdi, pokaži in pokaži, lahko pa stojiš.
Tako ozonuvannya s pravilnim pristopom - tse kompleksno čiščenje vode.

Za materiale http://voda.blox.ua/2008/10/Kak-vybrat-filtr-dlya-vody-34.html
Pri normalnih umivalnikih je ozon plinast, brez pusta govora, z volodjo ostrega vonja. Vvazhaêtsya, kjer je vonj ozona vonj sveže hrane, groziš. Vredno je torej, če je le v tem primeru koncentracija še nižja in postane del mejne dovoljene koncentracije (HDC). Podroben opis fizikalnih in kemijskih moči ozona je mogoče videti v numeričnih robotih, zokrem. deyakí glavni fizične in kemijske oblasti smernice za ozon v tabeli 1.1.
1.1. Osnovna fizikalna in kemijska moč ozona.
Odpornost na ozon v vodi
Ko se ozon določi v vodi, se njegova koncentracija postopoma povečuje in doseže mejne vrednosti za te pogoje (Voz / Vv) ali v absolutnih vrednostih za ozon (g / l). Hkrati je pomembno, da je postopek odločanja v skladu z Henryjevim zakonom, vendar je količina ozona sorazmerna z oprijemom plinam podobnega ozona nad raztopino.
Cstat = β M Pγ, g / l
De: Cstats - odpornost na ozon, g / l; β - Bunsenov koeficient; M - koncentracija ozona = 2,14 g / l; Pγ je delni oprijem ozona v odprtem plinskem okolju.
To pomeni, da je ozon odgovoren za glavne atmosferske pline - dušik in kislost, malo manj oksidantov, kot sta klor in klorov dioksid, raztapljanje ozona pa se pri nižjih temperaturah vode hitro spreminja.
Porazdelitev ozona v vodi
Eno uro se ozon dostavi v vodo. S široko hitrostjo prve kapljice je mogoče kot povečano vrednost "ure življenja" kopičiti v temperaturi vode in predvsem iz skladišča vode, predvsem zaradi manifestacije voda majhnih hiš, zlasti izvirov organskih kovin. Položaj blaga je treba ponazoriti s podatki, namenjenimi malemu 1.2. 
Malunok 1.2. ... Porazdelitev ozona v drugih vrstah vode pri temperaturah 20 ° C.
- Dvojno destilirana voda. 2. Destilat. 3. Voda "Z-pid pipe". 4. Voda jezera Tsurikhovskoye je bila filtrirana.
Ura življenja v enkratni destilirani vodi je 20 hilinov, v izredni vodi pa škropljenje s hilinom.
Reakcija na ozon z anorganskimi besedami.
Na ozon lahko reagiramo z rastjo, ki jo v vodi najdemo po dveh različnih mehanizmih: brez sredine kot ozon (v molekularni obliki) in v prisotnosti radikala OH *, kot vino, ko pade ozon v vodo. Vvazhaêtsya, scho v nevtralni vodi 2 kanala reakcij občasno rozpodіlenі. V kisli sredini ima ponovna fermentacija molekularni mehanizem, v leni pa radikalno. Ozonske madeže v kemičnih reakcijah, kot je oksidacija, je mogoče oceniti glede njegovega oksidativnega zdravja po tako imenovani velikosti oksidnega potenciala. Vrednosti vrednosti oksidacijskih potencialov malih rek in oksidacijskih potencialov so prikazane v tabeli 1.3.
oksidira |
Oksidacijski potencial (Volt) |
Predstavi. Oksli. potencial do OK pit. klor |
hidroksilni radikal |
||
atomska kislina |
||
Peroksid |
||
kloronuvatno kislino |
||
klorov dioksid |
||
Tabela 1.3. viplyaê, ozon je najmočnejše oksidant. Za stabilne govorce se uporablja samo fluor, hitrost reakcije na ozon je mogoče oceniti za grobe tekočine kot odziv nanje, količino reakcije na ozon pa je mogoče oceniti po količini reakcije Chastkovo tsí daní, predstavljeno otroku 1.3.
Reakcija na ozon s kovinami
Z lahkoto jih oksidirata z ozonom in manganovim hidroksidom ter manganovim dioksidom. Permanganat lahko za takšno reakcijo poda tudi izjave: 2Mn + ² + 5O3 + 3H2O □ 2MnO4ˉ + 3O2 + 6H + Vzporedno s procesom cim se izvaja proces - izguba mangana iz območja:
2Mn + ² + 2O3 + 4H2O □ 2MnO (OH) 2 ↓ + 2O2 + 4H + Oksidacija ionov v manganovem oksidu, kobaltu in niklju se uporablja v tekočinah, saj so vrednosti likvidnostnih konstant 1 / tekočina podane po vrstnem redu velikosti. Krom se lahko oksidira v šesvalentni krom. Proces zlaganja, vimag posebnih umov. 5 6 Svinec oksidiramo z ozonom PbO2 s reakcijsko konstanto blizu 10 -10 l / mol sek. Kovine, ki tvorijo komplekse z EDTA, na primer Pb, Ni, Cd in Mn, včasih gredo skozi fazo uničevanja kompleksa in nato oksidirajo. Takšne reakcije nastanejo zaradi kompleksacije kovin z naravnimi huminskimi kislinami.
Reakcija na ozon organske žleze.
Elektronska struktura bipolarnega ozona: z ene strani negativna, z druge pozitivna. Ozon se lahko hkrati odzove tako elektrofilno kot nukleofilno, podobno pa se v reakciji neposredne oksidacije rek z ozonom v vodi spremeni elektrofilni mehanizem. Rozumovskiy. Zelo pomembno je podati značilnost reakcije vseh glavnih organskih stavkov z ozonom. Če pogledamo neposredno v ozon, je to mogoče sedežu: Nazivne alkoholne spojine še pogosteje reagirajo z ozonom. Večina kloriranih v ogljikovih hidratih in navit, nenasičenih v ogljikovih hidratih ne reagira brez ozona. Na splošno je treba posredovati pri interakciji z ozonom preko OH radikala. Benzen ozon oksidira pogosteje, policiklični v ogljikovih hidratih pa več.
Ura reakcije na ozon s fenolnimi polovicami postane nekaj sekund. Chastkovo reakcijska shema za fenol je predstavljena na malem 1.5. Ionski fenat reagira hitreje, manj protoniranega fenola. To pomeni, da je konstantna hitrost še večja in blizu fenolom Riznoi Budovia. Karboksilne kisline, ketične kisline in številni podobni izdelki so stabilni produkti v procesu oksidacije organskih tekočin z ozonom. Amini pri nevtralnih vrednostih pH reagirajo z ozonom, pri pH> 8 oksidacijske reakcije potekajo hitreje. Vendar pa reakcija oksidacijskega aminiva v glavnem poteka skozi OH radikale. Četrtinski aminis (aromatski aminis) reagirajo z ozonom shvidshe. Alkohol lahko medsebojno deluje z ozonom, kar omogoča vmesni spojinski hidroperoksid. S celim smradom se oksidira v karboksilne kisline, tako kot drugi alkoholi v ketone. Ogljikove kisline šibko reagirajo z ozonom ali ne reagirajo z ozonom.
Merkaptan oksidira z ozonom v sulfonske kisline. Bisulfit in sulfonov Aminokisline pred skladiščem, ki vključujejo sirko (cistein, cestin in metionin), hitro reagirajo. Aminokisline (skladiščni del bilkiva) reagirajo z električnim mehanizmom. Med pesticidi je za maščevanje estra fosforne kisline najboljša oblika paration. Ozonuvannya tsyogo zêdnannya za proizvodnjo pred pojavom paraoksona, ki je bolj strupen, z nizkim parationom. Nadaljnje ozoniranje ponovno pretvori paraokson v manj strupen govor (na primer v nitrofenol, ki se nato oksidira v končne produkte - nitrat in CO2).
Pri vzorčenju pitne vode je mehanizem neposredne oksidacije skozi ozon v molekularni obliki osnovni. Konstante velikega števila organskih snovi z ozonom so predstavljene v reviji Hoigne.
- Ozon kot aktivator mikroflore.
Takoj, ko se hrana pokvari, bo ozon prisilil baktericidno in virulentno (protivirusno) delovanje. dobre ocene Učinkovitost mladih razkužil dobro ponazarjajo podatki dečka 2.1.

Malunok 2.1. Hitrost dekontaminacije patogenih E-coli z različnimi deaktivirnimi sredstvi.
V dani uri se pri ocenjevanju učinkovitosti tega dezinfekcijskega sredstva imenuje kriterij Z x T, tako da se koncentracija reagenta prilagodi za eno uro. Lahko rečemo, da je DIA (inaktivacija) = koncentracija Ura izpostavljenosti Tabela 2.1. za ustrezno vrednost meril SHT za majhne mikroorganizme - razkužila Tabela 2.1. Merilo CGT za majhne mikroorganizme (99% inaktivacija pri 5-25 ° C. Merilo CGT (Mb / L xv))
pogled na mikroorganizme |
PH ozona: 6/7 |
PH vilnega klora: 6/7 |
PH kloramina: 8/9 |
Klor -dioksid pH: 6/7 |
poliovirus |
||||
rotavirusi |
||||
Gardialyamblasti |
||||
Gardia myurism |
||||
Kriptosporidij |
||||
Za 90% inaktivacijo (1 dnevnik) |
Ozon očitno preglasi takšna razkužila, kot so klor, kloramin in klorov dioksid.Za takšno patogeno, kot je črevesna palica (E-coli), je ozon učinkovitejši, manj klora, malo več. Iste ure se za kriptosporidij merila za razkužila približajo do 1000. Za prenos načeloma lahko ozon tekmuje s takšnimi razkužilnimi reagenti, kot so klor, brom, jod, klorovodikova kislina., Vyroblyayu klorovodikova kislina HOCl, jaka, po lastni volji, disociacija v vodi za generalnega direktorja aniona in kationa N. Ugotovljeno je bilo, da je pri pH = 8 koncentracija neraztopljene kisline ≈ 20%, pri pH = 7 pa koncentracija HClO ≈80%. Ker je torej močan baktericidni učinek nizke HCLO, je treba z vikorijanovim klorom (v prisotnosti hipoklorita) zmanjšati optimalno vrednost pH. niso primerni za propadanje po vodi. Zaradi dezinfekcijske moči je jod šibkejši od klora in več kot ozon, vendar je učinkovitejši pri transportu. Nizka vrednost GDK. Težava je v odobritvi bromatov, kadar so ozonirani z bromom; Vendar se lahko zdi, da so vse smrdi kot pomanjkljivosti in velik podaljšek do današnje ure. " V danski uri se klor opere v posebni napravi-klorat, pri elektrolizi kuhinjske soli ali hipoklorita, ki ga najdemo v vodi, pa je potrebna koncentracija prostega klora. Na splošno je treba izraz "močan klor" povečati koncentracijo klorirane kisline in HClO. Za testiranje kloratorjev je potrebna zaloga reagenta, hipoklorit pa, ko se razgradi, izpusti klor. - Klor, odpadni plini (GDK za klor je 1 mg / m³). Win vpershe buv vikoristaniy yak boyova otruyna zasib in persha svitovu víynuŽrtev tega nasilnika je veliko.Ozon lahko razvrstimo med strupene pline, HDC pa lahko doseže nizko raven (0,1 mg / m³). Na srečo ima ozon super močan značilen vonj in ljudje zaznajo prisotnost ozona v nekaterih prejšnjih, nižjih koncentracijah, ki so še vedno nevarne (čas vonja ≈ 0,1 / 0,5 GDK). Pred današnjo uro izjemno smrtonosnega je treba poskrbeti za pomembno, ki je v bolnišnici, vodka dezon ozon. Hranilna toksičnost ozona ne bo obravnavana ločeno. Eno glavnih neprimernih moči klora je, da v primeru reakcije z velikim številom organskih spojin spekter organoklorovih otrok, veliko število klora in strupenih strupov .Od najmočnejših vrst na Danskem bo prišlo do nekaterih organskih kršitev, poleg tega pa bo v uničenem imunskem sistemu v populaciji veliko toksinov. Torej, ko govorimo o dioksinih, inodi vikoristovuyt izraz "kemični SNID." Precej govor je mogoče opraviti s šibkim razkužilom in nekoliko površno močno dražiti sluznico oči in nazofarinksa.Kloramini pogosto imenujejo "vezani s klorom". Celotna paleta klorovih prelivov je 5-10-krat močnejša promotorka, manj klora.Ozon se lahko uporablja tudi za industrijsko uporabo (stranski proizvodi) za ozoniranje plina in kondenziranih zmesi. Teoretično je mogoče priznati, da ga sprejemajo izdelki, ki so bolj strupeni, z manj ozona. Ta problem je bil predmet že pred mnogimi leti. Koncentracija in skladišče industrijskih rek, ki jih zaznamo pri ozonizaciji, celo ležijo zaradi dejstva, da je voda ozon. Noro, prvo mesto za pretvarjanje, da je manj izdelkov in skladišče je bolj očitno. Vsa hrana bo gledana iz splošne distribucije. Možno je povzeti, da se hrana bagatorijev konča do naslednjega ranga:
- Velika večina industrijskih proizvodov, oksidiranih z ozonom, je manj strupenih, manj strupenih.
- Neposredno povezovanje vmesnih govorov, ki so bili izvedeni med poskusnimi poskusi s kloriranjem in ozoniranjem, je pokazalo, da je v prvi vrsti bolj pomembno, da se pretvarjamo, da so bolj produkti.
2.1. Dezinfekcija klora in ozona na industrijskih čistilnih postajah in v laboratorijih.
Bagatorska zgodovina registracije dveh razkužil v velikih čistilnih napravah za maščevanje bogatega dejanskega gradiva, tako da lahko sodimo o njihovih prehodih in pomanjkljivostih. Številni številni primeri nastajajo pri dnu "Ozonuvannya Vody"
Na filtrirni postaji Belmont v Philadelphiji (ZDA) je ozoniranje vode dalo uspešnejše rezultate v smislu e-coli, manjše rezultate pa je bilo doseženo s kloriranjem. Učinek onesnaženja vode z ozonom v primeru ekstravagantnih količin bakterij v 1 ml 800-1200 od. postati: v odmerku 1 ml / l ozona - 60-65%, v odmerku 2 ml / l - 85%, v odmerku 3 ml / l - 90-95%. Na vodovodni postaji Rublevskaya (podzemna postaja Moskva) je bila 3-4 ml / l dodana sprejemljiva doza ozona. Ozoniranje voda Moskovskih rek je bilo izvedeno. Količina bakterij v 1 ml vode se je med 1-2 urami zmanjšala za 92-99%. Baktericidni odmerek ozona je bil dan kot polnilo, ki ga ni mogoče e-coli v 500 ml. voziti. Prilagoditev nesreče od 6,8 do 12 mg / l in obarvanost od 3,2 do 18 Greden. Inimal za povečanje baktericidnega odmerka ozona s 3,2 na 4,1 mg / L. Postaji "Rydenor" in "Ingols" iz ZDA smo v destilirani vodi pri Hp = 6,8 in pri temperaturi dolili suspenzije klora in ozona e-coli 1 ° C, tako da 99% kolonij e-coli odmre, so postale 0,25-0,3 mg / l za 16 minut za klor in 0,5 mg / l za 1 minuto za ozon. Graf 2.3. razvidno je, da je krivulja bakteriološkega upada posledica povečanega odmerka klora, poleg tega pa obstaja približno eksponentno zmanjšanje števila bakterij. V primeru ozoniranja obstaja slika - pri nizkih koncentracijah ozona je količina ozona v bakteriji zanemarljiva, vendar se popravi iz zelo kritičnega odmerka (0,3-0,5 mg / l), ozon se znatno poveča in poveča količino v določenem delu klora v mikroflori Ozon je potreben za baktericidno delovanje. pevska ura... Hkrati je celotna masa bakterij ozon. Klor viroblyaê vibіrkovе otrunnya zhitєvyh centrov bakterij, poleg tega je treba dodati še več po potrebi za trivialno uro za razpršitev v protoplazmi.
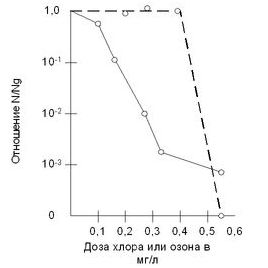
Graf preživetja bakterij med obdelavo vode z ozonom in klorom----ozon -------- klor
2.4. Diya ozon na supertokih, cistah in drugih patogenih.
Ozon je tudi učinkovito bakterijsko sredstvo v smislu mikroflore. Po Bringmannu je bil Bacillus subtilis nagnjen k ozonu v vodi 3000 -krat več, manj klora. M. Kane in Glöckner sta injicirala ozon in klor v ciste (tanke membrane, ki so postavljene na približno enovrstnih organizmih) Endamoeba hystolica v bakterije, podtipe kultur. Nameščeno približno eno uro, je potrebno za izčrpavanje cič organizmov s presežno koncentracijo ozona 0,3 mg / l, skladišče 2-7,5 minut in za klor (presežna koncentracija 0,5-1 mg / l) za več klora - 15-20 minut.
Diya ozon na virusu
Ozon nadaê yaskravo virazhene, radikalno infuzijo številnih virusov, ki jo nadzira vedno več puhanja virusnih beljakovin. V štiridesetih in šestdesetih letih prejšnjega stoletja so ameriški virusologi in Nimechchines izvedli številne dodatne teste z suspenzijami poliemilitnega virusa z dodatkom dodatnega klora, ozona in klorovega dioksida. Risbe od tsikh do sihdzhen lahko predstavimo v žaljivem pogledu:
- Inaktivacijo virusa polioemilite s klorom lahko dosežemo v odmerku 0,1 mg / l pri temperaturi vode 18 ° C, pri temperaturi vode 7 ºC, odmerek klora ni manjši od 0,25 mg / l.
- Inaktivacijo virusa za dodaten ozon lahko dosežemo z odmerkom 0,1 mg / l pri temperaturi vode 18 ° C, za hladno vodo pri -7 ° C je odmerek posledica, vendar se poveča na 0,15 mg / l.
- V primeru vikorijevega dikoksida potrebuje klor odmerek 0,6 mg / l (18 ºС). Za vodo s temperaturo 7 ºС je odmerek klorovega dioksida odgovoren za 1 mg / l.
Po Naumannovem poklonu je potreben poliemilit zenizyutsya ozon 2 minuti pri koncentraciji 0,45 mg / l, enkrat na uro kloriranja z odmerkom 1 mg / l 3 leta.
Ozon in hidrobionti
Po mnenju številnih avtorjev je ozon uspešno asimiliral mikro-hidro-rast in enostavnejši, aktivnejši in manj klora. Tako je ozon pri koncentraciji 15 mg / l 3 minute najpreprostejši, saj ohrani svojo aktivnost, če ga vzorčimo z odmerkom klora 250 mg / l trivialno uro. Pri odmerku 0,9-1,0 mg / l ozona so se ličinke dresenije mehkužcev izgubile 90%, pri odmerku 2 mg / l - 98%, pri odmerku 3 mg / l - povečale. Daljše oblike mehkužcev so bile izgubljene, ko so bile z ozonirano vodo (do 30 minut) bolj nepomembne. Res je, veliko vode, ki jo želite divje rasti v bližini zelo kritičnih bazenov na zaspanih lučeh, šibkih do ravni ozona. Tu vikoristovuyut udarne odmerke klora. Čiščenje ponoči med preventivnim čiščenjem takšnih bazenov.Z dovajanjem vrečk z izjemno kratkim ozonom, klorom in klorov dioksidom kot sredstvom za čiščenje in razkuževanje vode očitno Díysní, da vidim robote čistilnih naprav, ki bodo víkrístovuyut ozon in klor, bom povečal zmanjšanje ozona v cimet. Tako V. F. Kozhinov, ki je postavil francosko postajo za pripravo vode v Saint-Maureu in postajo v Chicagu (ZDA), pomeni, da je bil prvi padec bolezni "vodnih potovanj" registriran v 1 padcu na 100 tisoč. Prebivalci, ki želijo koncentracijo presežnega ozona v vodi, niso presegli 0,05 mg / l. Iste ure je bilo v Chicagu majhno mesto bolezni črevesne bolezni črevesja, na katerega klor ni vplival daleč od oskrbe z vodo.) Taku je pomislil: "Najbílsh іstotnyh zaprechennya proti ozonuvannya zvvazyayut vívazhayut vídnítní presežek ozona v ozonu pri razdeljevalni fenestraciji pri oskrbi z vodo, tako da za uro kloriranja v količini kopičenja presežka. " Poskusi, izvedeni v Ashtonu (Anglija), so pokazali, da v razkuženi z ozonom vodo, ki kroži po referenčnih vodovodnih cevovodih, ne pride do poslabšanja kakovosti. Kontrolni vzorci ozonske vode, vzeti iz žive meje, so se izkazali za popolnoma enake vzorcem, ki so bili odvzeti iz dzherela, tako da je bilo mogoče presežek klora odstraniti v vodi. To pomeni, da prisotnost presežka klora v cevovodih ne pomeni enake bakterijske čistosti vode. Eden od avtorjev se je o težavi pogovarjal z voditelji vodovoda Tsurikhovsky in odobril misel, da so dezinfekcijska sredstva za prenos ozona M.T.B. nesporna. Zaradi moči ne bom gledal ozona. Nareshti, problem partotičnosti. Mislim, da je ozonuvannya veliko dražja od chloruvannya. Vendar ni tako. V procesu kloriranja vina je treba klor dati v vodo, izvesti tako imenovano dekloriranje. Za odstranjevanje vode in dobre kakovosti se dela in uporabljajo posebni reagenti. Zaradi poslabšanja faktorja, pa tudi zaradi tendence neprekinjenega zniževanja cene oskrbe z ozonom in podražitve klora in klorovih izdelkov, je v tej uri pogostost teh procesov primerljiva. Na kaj? Є več razlogov: - psihološki razlog. Pratsyuvati s klorom, še posebej, ko gre za balone z rdečim klorom, je precej preprosto. Za dostavo zračnikov balona ali kapacitete v bazen v obliki hipoklorit, kot vse težave z dezinfekcijo virusa. Cena, nora, enostavnejša, brez iskanja koncentracije ozona, kako iti od ozonatorja, vendar je ozonator ohlapno prepognjen in ga moramo spremeniti, vendar ga ni mogoče izklopiti. Razširitev na ozon. Do zadnje ure je bila potreba po posesti ozonatorja prevelik pankrt in nizka stopnja avtomatizatsії pripuskayut neobhіdnіst vikoristannya obslugovuyuchogo osebje schodo visokoї kvalіfіkatsіі.Suschestvenny preboj v problemі stvorennya nadіynogo, neroden v vikoristannі ozoniranje i ozonoіzmerіtelnogo obladnannya je mozhlivim pіslya pojavil Suchasnyj IGBT tranzistorіv scho so dovoljene rіzko sprostiti i zdesheviti virobnitstvo іmpulsnih visokovoltnih generatorіv, rozvitok mіkroprotsesornoї tehnіki i novih tipіv ultrafіoletovih senzorji, posebni sintetični zeoliti in v. Vse cene in rezultati zamude impulznih električnih razelektritev v preteklosti so omogočili razvoj tehnološke rešitve Uvedli smo nove možnosti za proizvodnjo ozonatorjev v sušeni hrani, kislinskih ozonatorjev, sistemov za spremljanje presežka ozona v vodi, ozonometra, kisnyu koncentrator To je najboljša lastnost, kako preprečiti ozonuvannya zonuvannya nagato bolj odpustiti in priročno tehnologijo, vendar ne prej. Naši radijski sprejemniki, naša zadnja generacija in distribucija, ki so jih zasegli patenti v Rusiji, ZDA, na Japonskem in v drugih državah, bodo brez blagoslova pomagali življenju preprostejših ljudi in pomagajmo jim.
Seznam literature
Draginsky V.L., Aleksova L.P., Samoilovich V.G. "Ozonuvannya v postopkih čiščenja vode" M. Deli print. 2007 r
Інж. V.V. Karaffa-Korbutt "Ozon 'in jogo zasosuvannya V industriji in sanitarni" Ed. SPP "Osvita". 1912 RUR
V.F. Kozhinov, I.V. Kozhinov "Ozonuvannya Vodi" M. Stroyizdat 1973 r
V.V. Lukin, M.P. Popovich, S.N. Tkachenko "Fizikalna kemija do ozona" Ed. MSU 1998r.
Manley T.S., Negowski S.J. Ozon v enciklopediji kemijske tehnologije. Drugo izd. Letnik 14. N.J. +1967.
Hozvath M. H., Bilitrki, haud., Huttez. "Ozon" Ed. Akademija. Kiado. Budimpešta tisoč devetsto šestinšestdeset sedem
Kogan B.F. jaz br. "Dovidnik o razčinnosti" v.1, knj. 1, M. tisoč devetsto enainšestdeset.
Masschelein W.J. "Proces unitaixes du Treatmeut de l esu potable" Ed. CEBEIOC. Hiege. 1996.
Jore M., hegube B.J. Er. Hydrol. 14.11.1983.
Cowen W. Fetal. "Kemija pri ponovni uporabi vode". Ed. Ann. Azboz. Science Publ. Michigan. 1985.
Curol M.D. Env. Prog. 4.46.1985.
Hoigne J. "In Progress Technologies for water treatment" Ed. Plenum. Pritisnite # 3. +1988
Rozumovskiy S.D. і Zaika G.Z. "Reakcije ozona in joga z organskimi spojinami" M. 1974.
Hubner R. Gesundheitstechnik št. 12. 1973.
Dojbido J. Etol. "Osvita industrijskih rek v procesu ozoniranja in kloriranja" Wat. Res. 1999. 33. št. 4 р3111 - 3118.
Ridenour G.M., Inglols R.S. Ameriški zbornik za javno zdravje 1946. 3.6p 639.
Gomella C. 2e treitment d eux par l ozon. Izvleček du mensuel du ceutre Belge 287.1,967.
Kozhinov V.F. Ozonuvannya vodi. "Miske Gospodarstvo Moskvy" 1970. št. 7.
Steinhardt. Državna higiena. 1S. 1956.
Naumman E. "Das gas nnd Wassertach" 1952. NY.p. 81.
Dickerman J.M. etral. Journ of New England Water Works Ass. 1.11.1954.
Shalashova E.S. "Imenovanje ozona za čiščenje vode s strani države" №6. 1960.
Thorp C. E. Jnd Med in Surg. 1950. v19 str 49
M.U. 2.1.2.694-98. "Vikoristannya ultravijolično vimírí v primeru okužene vode bazenov".
G.I. Rogožkin. "Čiščenje in okužba vode v bazenih" Santekhnika. 4.2003. stran 4-9.
